
一定能在下列溶液中大量共存的离子组是( )
①含有大量Al3+的溶液中:Na+、NH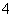 、SO
、SO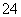 、Cl-
、Cl-
②加入Al能放出H2的溶液中:Cl-、HCO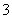 、SO
、SO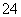 、NH
、NH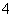
③含有大量Fe3+的溶液中:Na+、Mg2+、NO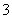 、SCN-
、SCN-
④在含有大量AlO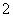 的溶液中:NH
的溶液中:NH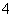 、Na+、Cl-、H+
、Na+、Cl-、H+
⑤由水电离出的c(H+)=1×10-14mol·L-1的溶液中:Ca 2+、K+、Cl-、HCO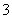
A.①② B.①③⑤
C.① D.①④⑤
科目:高中化学 来源: 题型:
硫酸钠-过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:①准确称取1.770 0 g样品,配制成100.00 mL溶液A。②准确量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.5825 g。③准确量取25.00 mL溶液A,加适量稀硫酸酸化后,用0.020 00 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液25.00 mL。H2O2与KMnO4反应的离子方程式如下:2MnO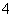 +5H2O2+6H+===2Mn2++8H2O+5O2↑
+5H2O2+6H+===2Mn2++8H2O+5O2↑
(1)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO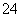 )≤1.0×10-6 mol·L-1,应保
)≤1.0×10-6 mol·L-1,应保 持溶液中c(Ba2+)≥________mol·L-1。
持溶液中c(Ba2+)≥________mol·L-1。
(2)上述滴定若不加稀硫酸酸化,MnO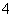 被还原为MnO2,其离子方程式为______________。
被还原为MnO2,其离子方程式为______________。
(3)通过计算确定样品的组成(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关氯气的叙述中正确的是( )
A.氯气在常温下能与铁反应,故不能用铁罐存放液氯
B.液氯和氯水是同一物质
C.点燃氢气和氯气的混合气体可以制取氯化氢
D.氯气跟变价金属反应生成高价态金属氯化物
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,下列各组离子在指定溶液中可以大量共存的是( )
A.由水电离出的c(H+)=10-12mol/L的溶液中:Na+、Ba2+、HCO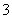
 、Cl-
、Cl-
B.无色透明溶液中:K+、2n2+、SO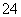 、Na+
、Na+
C.含有大量AlO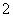 的溶液中:Na+、OH-、Cl-、CO
的溶液中:Na+、OH-、Cl-、CO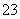
D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、SO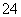
查看答案和解析>>
科目:高中化学 来源: 题型:
在灾后重建中,饮用水安全占有极为重要的地位, 某研究小组提取三处被污染的水源进行分析,并给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E五种常见化合物都是由下表中的离子形成的:
| 阳离子 | K+、Na+、Cu2+、Al3+ |
| 阴离子 | SO |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液。
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解。
③进行焰色反应实验,只有B、C含有钾离子。
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀。
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验现象填写下列空白:
(1)写出B、C、D的化学式:B________、C________、D________。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为________。
(3)写出实验②发生反应的离子方程式________________________________________
________________________________________________________________________。
(4)C常用作净水剂,用离子方程式表示其净水原理_______________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列说法正确的是( )
A.白色沉淀是CuI2,棕色溶液含有I2
B.滴加KI溶液时,转移1 mol电子时生成1 mol白色沉淀
C.通入SO2时,SO2与I2反应,I2作还原剂
D.上述实验条件下,物质的氧化性:I2>Cu2+>SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是( )
A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,水解程度越大
D.同周期金属元素的化合价越高,其原子失电子能力越强
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:① 2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1 ②H2(g)+S(g)=== H2S(g) ΔH=-20.1 kJ·mol-1。
下列判断正确的是( )
A.1 mol氢气完全燃烧生成液态水吸收热量241.8 kJ
B.1 mol H2O(g)和1 mol H2S(g)的能量相差221.7 kJ
C.由①②知,水的热稳定性小于硫化氢
D.若反应②中改用固态硫,1 mol S(s)完全反应,放出的热量小于20.1 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1︰1︰1时,实际参加反应的FeS与HNO3的物质的量之比为( )
A.1∶6 B.1∶7 C.2∶11 D.16∶25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com