
| A. |  | B. |  | ||
| C. | 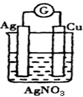 | D. | 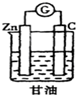 |
分析 构成原电池需具备以下条件:两个活性不同的电极;电解质溶液;形成闭合回路;存在能自动发生的氧化还原反应,且为放热反应,以此来解答.
解答 解:原电池的构成条件是:1、有两个活泼性不同的电极,2、将电极插入电解质溶液中,3、两电极间构成闭合回路,4、能自发的进行氧化还原反应;
A.酒精不是电解质,所以不能构成原电池,故A错误;
B.没有形成闭合回路,所以不能构成原电池,故B错误;
C.满足原电池构成的条件,能构成原电池,故C正确;
D.甘油是非电解质,没有电解质溶液不能构成原电池,故D错误.
故选C.
点评 本题考查了原电池原理的分析应用,属于基础性试题的考查,难度不大,明确原电池的工作原理、构成条件是答题的关键.


科目:高中化学 来源: 题型:解答题
 氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示;
氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示;查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③④ | C. | ③④⑤ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 酸或碱 | 电离常数(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 6.2×10-10 |
| HClO | 3×10-8 |
| NH3•H2O | 1.8×10-5 |
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1.1×10-10 |
| BaCO3 | 2.6×10-9 |
| CaSO4 | 9.1×10-6 |
| CaCO3 | 2.8×10-9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com