
【题目】对于反应:4P+3KOH+3H2O===3KH2PO2+PH3,已知PH3的P的化合价为-3,磷单质在反应中
A.被氧化B.被还原
C.既被氧化又被还原D.既未被氧化又未被还原
科目:高中化学 来源: 题型:
【题目】以乙炔为原料在一定条件下可转化为乙烯基乙炔(CH≡C—CH=CH2)。下列关于乙烯基乙炔分子的说法错误的是( )
A. 能使酸性KMnO4溶液褪色
B. 1 mol乙烯基乙炔能与3 mol Br2发生加成反应
C. 乙烯基乙炔分子中含有两种官能团
D. 等质量的乙炔与乙烯基乙炔完全燃烧时耗氧量不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图一图二分别表示某大分子的部分结构,回答下列问题。

(1)核酸是由____________连接而成的长链,其中DNA的基本结构单位有_______种。若图一表示某DNA分子单链片段,与组成RNA的基本结构单位相比,一定不同的是___________(填标号)。
(2)若图一表示某RNA分子的长链片段,则由①②③组成的物质称为______________。RNA中不含有的碱基是_____________。
(3)若图二中表示的多聚体是纤维素,则它的单体是___________,其与果糖缩合失去1分子水后形成的物质是_____________。若图二多聚体具有免疫功能,在不考虑其他单体连接的情况下,形成上述多聚体的过程中,相对分子质量减少了___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 常温常压下,48g O2和O3的混合气体中含有氧原子数为3NA
B. 17 g氨气所含质子数目为11NA
C. 标准状况下22.4L的四氯化碳,含有四氯化碳分子数为NA
D. 物质的量浓度为0.5 mol·L-1的MgCl2溶液中,含有Cl-个数为1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式不正确的是( )
A.铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑
B.氢氧化钠与盐酸反应:OH﹣+H+═H2O
C.锌与硫酸铜溶液反应:Zn+Cu2+═Zn2++Cu
D.氯化钡溶液与稀硫酸反应:Ba2++SO42﹣═BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.3 mol NH3分子中所含原子数_____ ,质量是____,标准状况下的体积是____。
(2)含有0.4 mol Al3+的Al2(SO4)3溶液中所含SO42-的物质的量是______。
(3)等质量的SO2和SO3中, 硫原子个数之比为____,氧原子个数之比_______。
(4)配制100 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O质量为__________ ;0.5L0.5mol/L FeCl3溶液中的Cl-的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaCl2·xH2O是用途广泛的基础化工产品。我国目前主要是用盐酸和硫化钡(含少量Mg2+、Fe3+等)反应生产BaCl2·xH2O,工艺流程如下图所示。
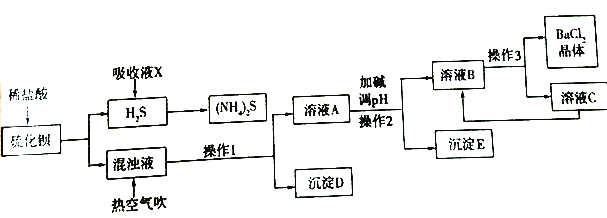
已知:室温时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]= 4.0×10-38
请回答下列问题:
(1)写出氯化钡的电子式________。盐酸和硫化钡反应的化学方程式为________。
(2)吸收液X的溶质是________。一定条件下向(NH4)2S溶液中通入空气,可得到单质硫并使吸收液再生,吸收液再生反应的化学方程式为________。
(3)操作1的名称是________,操作3的过程是将容液B蒸发浓缩、________、过滤等。
(4)沉淀D的成分是________。
(5)热空气吹除时会有部分HS-转变为S2O32-,使产品仍达不到纯度要求,可再进行酸化脱硫,酸化脱硫时的离子方程式为________。
(6)室温时,若加碱调溶液pH至9,则完全沉淀的离子是________ 。
(7)此工艺流程中循环利用的物质是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害。
Ⅰ.SO2的尾气处理通常有以下几种方法:
(1)活性炭还原法 反应原理:恒温恒容时2C(s)+2SO2(g)![]() S2(g)+2CO2(g)。反应进行到不同时间测得各物质的浓度部分图象如图:
S2(g)+2CO2(g)。反应进行到不同时间测得各物质的浓度部分图象如图:

①0~20 min反应速率表示为v(SO2)=________;
②30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是________;
③40 min时,平衡常数K=________。
(2)亚硫酸钠吸收法 ①Na2SO3溶液吸收SO2的离子方程式为__________________;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是___(填序号)。
a.c(Na+)+c(H+)>c(![]() )+c(
)+c(![]() )+c(OH)
)+c(OH)
b.水电离出c(H+)=1×108 mol/L
c.c(Na+)>c(![]() )>c(H+)>c(
)>c(H+)>c(![]() )
)
(3)电化学处理法

①如图所示,Pt(Ⅰ)电极的反应式为__________________;
②当电路中转移0.02 mol e时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加____mol离子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com