
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
| A. | 3.2g | B. | 6.4g | C. | 12.8g | D. | 21.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚丙烯的结构简式: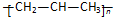 | B. | 二氧化碳的电子式: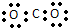 | ||
| C. | 乙酸的分子式:CH3COOH | D. | 中子数为18的硫原子:3416S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | VIIA族元素的非金属性:F>Cl,所以VIIA族元素氢化物的酸性:HF>HCl | |
| B. | 第二周期元素氢化物稳定性:HF>H2O,所以第三周期元素氢化物稳定性:HCl>H2S | |
| C. | 第二周期主族元素最外层电子数从1递增至7,所以第二周期主族元素的最高化合价也从+1递增至+7 | |
| D. | 工业制取金属钾的反应为:KCl (1)+Na (1)$\frac{\underline{\;850℃\;}}{\;}$NaCl(1)+K(g),所以金属性:Na>K |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| B. | pH=1的溶液中:Na+、Fe2+、NO3-、SO42- | |
| C. | 由水电离的c(OH-)=10-13mol•L-1的溶液中:Na+、Cl-、CO32-、NO3- | |
| D. | 能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 1 mol•L-1的Fe2(SO4)3 溶液加热蒸干得到Fe(OH)3胶体粒子的数目为2NA | |
| B. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1 NA | |
| C. | 0.1 L 0.5 mol•L-1 CH3COOH溶液中含有的氢离子数目小于0.05NA | |
| D. | 电解精炼铜时,若阴极得到电子数为2 NA个,则阳极质量减少64 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (c-a-b)kJ | B. | (a+b-c)kJ | C. | (2c-a-b)kJ | D. | (2c-a-b)/2 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com