
下列溶液一定呈中性的是 )。
A.cH+)=cOH-)=10-6 mol·L-1的溶液
B.pH=7的溶液
C.使石蕊试液呈紫色的溶液
D.酸与碱恰好完全反应生成正盐的溶液
科目:高中化学 来源: 题型:
设阿伏加德罗常数的值为NA,下列叙述正确的是( )
A.在铜与硫的反应中,1 mol铜参加反应失去的电子数为2NA
B.常温下,32 g含有少量臭氧的氧气中,含有的氧原子数为2NA
C.若1 mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA
D.78 g过氧化钠固体中所含阴、阳离子总数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应2SO2(g)+O2 (g) 2SO3(g),下列判断中正确的是( )
2SO3(g),下列判断中正确的是( )
A.2体积SO2和足量O2反应,生成 2体积SO3
B.恒温恒容,通入气体氦使压强增大,平衡向右移动
C.平衡时,SO2消耗速率等于O2生成速率的两倍
D.平衡时,SO2浓度等于O2浓度的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学科研小组研究在其他条件不变时,改变某一条件对可逆反应aA(g)+bB(g)  cC(g)化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,
cC(g)化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率, 表示体积分数)。根据图象,下列判断正确的是( )
表示体积分数)。根据图象,下列判断正确的是( )
A.反应Ⅰ:若p1>p2,则此反应只能在高温下自发进行
B.反应Ⅱ:此反应的ΔH<0,且T1<T2
C.反应Ⅲ:ΔH>0且T2>T1或ΔH<0且T2<T1
D.反应Ⅳ:T1<T2,则该反应不易自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
将NO2装入带活塞的密闭容器中,当反应2NO2(g) 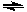 N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是 ( )
N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是 ( )
A.升高温度,气体颜色加深,则此反应为吸热反应
B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅
C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍
D.恒温恒容时,充入惰性气体,压强增大,平衡向右移动,混合气体的颜色变浅
|
温度/℃ | 1 | 2 | 4 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 )。
A.凡有能量变化的过程都是化学变化
B.吸热反应只有在加热的条件下才能进行
C.放热反应可能需要在加热的条件下才能进行
D.化学反应中的能量变化都只以热能的形式表现出来
查看答案和解析>>
科目:高中化学 来源: 题型:
燃烧热是指通常状况下1 mol纯物质完全燃烧生成稳定的氧化物所放出的热量。下列说法正确的是 )。
A.通常状况下,1 g氢气燃烧生成液态水时放出142.9 kJ热量,则表示氢气燃烧热的热化学方程式为2H2g)+O2g)===2H2Ol) ΔH=-571.6 kJ·mol-1
B.已知:H2g)+F2g)===2HFg) ΔH=-270 kJ·mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ
C.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3g),放热19.3 kJ,其热化学方程式为N2g)+3H2g) 2NH3g) ΔH=-38.6 kJ·mol-1
2NH3g) ΔH=-38.6 kJ·mol-1
D.已知:①Cs,石墨)+O2g)===CO2g) ΔH=-393.5 kJ·mol-1 ②Cs,金刚石)+O2g)===CO2g) ΔH=-395.0 kJ·mol-1,则Cs,金刚石)===Cs,石墨) ΔH=-1.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D、E,已知A、B为金属,C、D、E为非金属,C是最活泼的非金属,E与C同主族,D离子半径比E离子半径大。A、B的离子与C离子电子层结构相同,其中B离子的半径最小。下列有关说法错误的是
A.含氧酸的酸性: E>D B.原子半径:A>B
C.氢化物的热稳定性:C>E D.离子结合质子能力:D>E
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com