
【题目】【2016届临沂一模】工业上利用氟碳铈矿(主要成分CeCO3F)提取CeCl3的一种工艺流程如下:
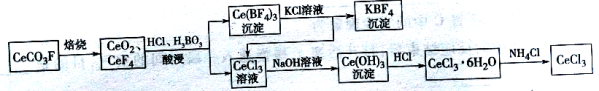
请回答下列问题:
(1)CeCO3F中,Ce元素的化合价为 。
(2)酸浸过程中用稀硫酸和H2O2替换HCl不会造成环境污染。写出稀硫酸、H2O2与CeO2反应的离子方程式: 。
(3)向Ce(BF4)3中加入KCl溶液的目的是 。
(4)溶液中的C(Ce3+)等于1×10-5mol.l-1,可认为Ce3+沉淀完全,此时溶液的pH为 。
(已知KSP[Ce(OH)3]=1×10-20)
(5)加热CeCl3 .6H2O和NH4Cl的固体混合物可得到无水CeCl3 ,其中NH4Cl的作用是____________。
(6)准确称取0.7500gCeCl3样品置于锥形瓶中,加入适量过硫酸铵溶液将Ce3+氧化为Ce4+,然后用0.1000mol.l-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗25.00ml标准溶液。(已知:Fe2++Ce4+=Ce3++Fe3+)
①该样品中CeCl3的质量分数为 。
②若使用久置的(NH4)2Fe(SO4)2标准溶液进行滴定,测得该CeCl3样品的质量分数 (填“偏大”、“偏小”或“无影响”)
【答案】(1)+3 (1分)(2)H2O2+2CeO2+6H+=2Ce3++4H2O+O2↑(2分,化学式写错、不配不得分,写化学方程式不得分)
(3)避免三价铈以Ce(BF4)3沉淀的形式损失或除去BF4-或提高CeCl3的产率
(2分,合理答案均得分)(4)9(2分)
(5)NH4Cl固体受热分解产生HCl,抑制CeCl3水解(2分,合理答案均得分)
(6)①82.2%或82.17% (2分) ②偏大(2分)
【解析】
试题分析:(1)CeCO3F中,CO32-是负二价,氟是负一价,则Ce元素的化合价为+3价;
(2)稀硫酸、H2O2与CeO2反应的离子方程式H2O2+2CeO2+6H+=2Ce3++4H2O+O2↑;
(3)避免三价铈以Ce(BF4)3沉淀的形式损失,应向Ce(BF4)3中加入KCl溶液;
(4)溶液中的c(Ce3+)等于1×10-5mol.l-1,可认为Ce3+沉淀完全,则KSP[Ce(OH)3]=1×10-20= c(Ce3+)c3(OH-)=1×10-5×c3(OH-),c(OH-)=10-5 mol·L-1,则c(H+)=10-9 mol·L-1,此时溶液的PH为9;
(5)加热CeCl3·6H2O得到无水CeCl3 ,加入了NH4Cl固体,因为NH4Cl固体受热分解产生HCl,可抑制CeCl3水解;
(6)①根据反应Fe2++Ce4+= Ce3++Fe3+及Fe2+的物质的量0.025×0.1=0.0025mol,得Ce3+的物质的量是0.0025mol,则样品中CeCl3的质量分数为(0.0025×246.5/0.75)×100%=82.2%;
②若使用久置的(NH4)2Fe(SO4)2标准溶液进行滴定,亚铁离子有可能被氧化,将会导致标准液体积偏大,CeCl3样品的质量分数将偏大。


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】下面列出了几组物质,请将物质的合适组号填写在空格上。
① 金刚石与石墨; ② 氧气(O2)与臭氧(O3);
③ 16O、17O和18O; ④ CH4和CH3CH2CH3;
⑤ 乙烯和乙烷;
⑥![]() 和
和![]() ; ⑦
; ⑦![]() 和
和 ;
;
(1)同位素 ,(2)同素异形体 ,
(3)同系物 ,(4)同分异构体 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学探究某有机物A的结构,进行如下实验:
①取6.0克A在氧气中完全燃烧,将生成气体依次通过M(装有浓硫酸)和N(装有碱石灰)洗气瓶,M增重7.2克,N增重13.2克。
②测定相对分子质量为60。
③测定核磁共振氢谱,有三个强峰,比值为6:1:1
据此回答下列问题:
(1)②中测定相对分子质量的方法为 ;
(2)写出A的分子式 ;
(3)A发生消去反应的化学方程式 ;
(4)A与乙酸反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】湿润的淀粉碘化钾试纸接触某气体而显蓝色,该气体可能是①Cl2 ②NO2 ③H2S ④SO2 ⑤溴蒸气 ⑥HCl中的 ( )
A.①④⑤ B.①②⑤ C.①②⑥ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:
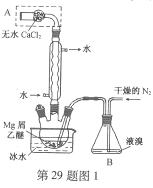

步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5
MgBr2·3C2H5OC2H5
请回答:
(1)仪器A的名称是____________。
实验中不能用干燥空气代替干燥N2,原因是___________。
(2)如将装置B改为装置C(图2),可能会导致的后果是___________。
(3)步骤3中,第一次过滤除去的物质是___________。
(4)有关步骤4的说法,正确的是___________。
A.可用95%的乙醇代替苯溶解粗品B.洗涤晶体可选用0℃的苯
C.加热至160℃的主要目的是除去苯D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++ Y4-====Mg Y2-
①滴定前润洗滴定管的操作方法是__________。
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是________________________(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届厦门一模】磷化氢( PH3)是一种剧毒气体,是最常用的高效熏蒸杀虫剂,也是一种电子工业原料。
(1)在密闭粮仓放置的磷化铝(AlP)片剂,遇水蒸气放出PH3气体,该反应的化学方程式为 。
(2)利用反应PH3+3HgCl2= P(HgCl)3 +3HCl,可准确测定微量的PH3。
①HgCl2溶液几乎不导电,说明HgCl2属于________________(填“共价”或“离子”)化合物。
②通过测定溶液____________变化,可测定一定体积空气中PH3的浓度。
(3)PH3的一种工业制法涉及的物质转化关系如下图所示: 
①亚磷酸属于________________元酸。
②当反应I生成的n(NaH2PO2):n(Na2HPO3) =3:1时,参加反应的n(P4):n(NaOH)= 。
(4)一种用于处理PH3废气的吸收剂成分为次氯酸钙80%、锯木屑(疏松剂)15%、活性炭2.5%、滑石粉(防结块)2.5%。
①次氯酸钙将PH3氧化为H3PO4的化学方程式为________________。
②空气中的水蒸气可加快PH3的氧化过程,其原因可能是____________。
(5)从(4)中的吸收残留物中回收磷酸氢钙(CaHPO4)的方法如下:
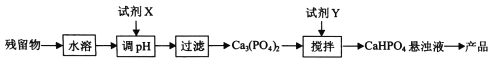
①试剂x为 (填化学式)。
②已知25℃时,H3PO4的Kal=7.5×10-3、Ka2=6.3×10-8、Ka3 =4.4×10-13。加入Y时,应控制悬浊液pH 7(填“>”、“=”或“<”),通过计算说明理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏伽德罗常数的值。下列说法正确的是
A.在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA
B.含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间
C.5NH4NO3![]() 4N2↑+2HNO3+9H2O中氧化产物比还原产物每多14g,转移电子数为15NA
4N2↑+2HNO3+9H2O中氧化产物比还原产物每多14g,转移电子数为15NA
D.用惰性电极电解饱和碳酸钠溶液时,电路上通过2mol电子时产生气体分子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届天津河东区二模】下表给出五种短周期元素的相关信息。
元素 | 相关信息 |
A | 常温、常压下,其单质是最轻的气体,它将成为备受青睐的清洁燃料 |
B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
C | 植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染 |
D | 室温下其单质为淡黄色粉末状固体,加热易熔化。该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
E | 常温下其单质为黄绿色气体,其单质水溶液有漂白、杀菌作用 |
请按要求回答下列问题:
(1)D元素核外电子排布 ;
(2)A、B两元素形成的含有非极性键的化合物的结构式 ;A、B两元素形成的具有相同电子数的离子有(填化学式):_____________、____________。
(3)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1∶2)一起用作火箭助推剂,两者发生反应生成无毒物质,写出上述化学反应方程式: 。
(4)一定条件下,在水溶液中1 mol E-、EOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。n是 (填离子符号)。离子反应y→x+m的热化学方程式为 。

(5)Na2DB3水溶液中各离子浓度的大小顺序是 (填离子符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2CH3COCH3(l)![]() CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是
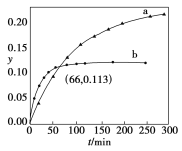
A.b代表0℃下CH3COCH3的Y-t曲线
B.反应进行到20min末,CH3COCH3的![]() >1
>1
C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的![]() =1
=1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com