
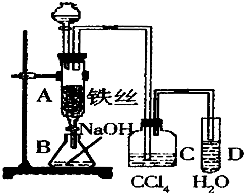
 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.分析 根据实验装置可知,将溴和苯的混合物滴入到铁丝上,在铁作催化剂的条件下苯和溴发生取代反应生成溴苯和溴化氢,溴和苯都是易挥发的物质,所以C装置中用四氯化碳吸收溴化氢气体中的苯和溴,生成的溴化氢用水吸收,注意要防止倒吸,所以导管口中液面上方,A中反应后的溶液放到B中,用氢氧化钠溶液除去溴苯中的溴,(1)铁与溴会生成溴化铁,苯和液溴在溴化铁催化作用下发生取代反应生成溴苯和溴化氫;
(2)溴化氢易溶于水,氢溴酸易挥发;
(3)溴能与氢氧化钠反应而溴苯不能;
(4)CCl4 能溶解溴不能溶解溴化氢;
(5)如果苯和液溴发生的是取代反应,则有HBr生成,如果发生的是加成反应,则无HBr生成.
解答 解:根据实验装置可知,将溴和苯的混合物滴入到铁丝上,在铁作催化剂的条件下苯和溴发生取代反应生成溴苯和溴化氢,溴和苯都是易挥发的物质,所以C装置中用四氯化碳吸收溴化氢气体中的苯和溴,生成的溴化氢用水吸收,注意要防止倒吸,所以导管口中液面上方,A中反应后的溶液放到B中,用氢氧化钠溶液除去溴苯中的溴,
(1)A中铁与溴会生成溴化铁,反应方程式为2Fe+3Br2=2FeBr3,在FeBr3的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有溴化氢生成:C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr,
故答案为:2Fe+3Br2=2FeBr3;C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr;
(2)由于溴化氢易溶于水,氢溴酸易挥发,所以D中可观察到有雾状物质出现,
故答案为:有雾状物质出现;
(3)溴单质能与氢氧化钠溶液反应而溴苯不能,反应方程式:Br2+2NaOH═NaBr+NaBrO+H2O,
故答案为:除去溶于溴苯中的溴;Br2+2NaOH═NaBr+NaBrO+H2O;
(4)CCl4 能溶解溴不能溶解溴化氢,四氯化碳能除去溴化氢气体中的溴蒸气和苯,
故答案为:除去溴化氢气体中的溴蒸气;
(5)如果苯和液溴发生的是取代反应,则有HBr生成,如果发生的是加成反应,则无HBr生成.也就是说,如果要证明苯和液溴发生的是取代反应,而不是加成反应,只需检验有无HBr生成.可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明发生取代反应,我们再回答出检验H+的方法即可,可用石蕊试液,若变红则发生取代反应.但溴易挥发,溴化氢气体中的溴蒸气对溴化氢的检验有干扰作用,因此,在检验溴化氢前必须除去溴蒸气,这也正是C中盛放的CCl4的作用,
故答案为:AgNO3溶液或石蕊试液;产生淡黄色沉淀或溶液变红色.
点评 本题考查苯的取代反应方程式及实验现象以及产物HBr的检验,题目难度中等,注意掌握苯的取代反应原理,明确反应的产物及HBr的化学性质进行解题.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的铁与稀H2SO4反应 | B. | FeO与H2SO4反应 | ||
| C. | FeCO3与H2SO4稀反应 | D. | Fe(OH)3与稀H2SO4反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr
+HBr| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸.
实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸. +NaOH→
+NaOH→ +
+
 (不容于醚,可溶于水)
(不容于醚,可溶于水)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
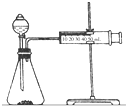 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol/L的硫酸于试管中;②分别投入大小、形状相同的Al、Fe、Mg | 反应快慢:Mg>Al>Fe | 反应物的性质越活泼,反应速率越快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2和Na2O都是白色固体,都能与冷水作用得到O2和NaOH | |
| B. | 在Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水 | |
| C. | 相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1 | |
| D. | Na2O与Na2O2都能与水反应生成碱,它们都是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最终酸性高锰酸钾溶液褪色 | B. | 反应中甲醛被还原 | ||
| C. | 最终酸性高锰酸钾溶液是红色 | D. | 说明甲醛是具有氧化性的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com