
| A. | 乙醇(C2H5OH)和乙烯 | B. | 丙烷和乙醛(CH3CHO) | ||
| C. | 乙烯和乙酸乙酯(CH3COOC2H5) | D. | 甲醛(HCHO)和葡萄糖(C6H12O6) |
分析 无论以何种比例混合,只要混合物的总质量一定,完全燃烧生成H2O的质量也一定,则说明混合物各组分分子中含氢量相等,据此对各选项进行判断.
解答 解:A.乙醇分子式为C2H6O,氢元素的质量分数为$\frac{6}{46}$=$\frac{3}{23}$,乙烯分子中含氢量为:$\frac{4}{28}$=$\frac{1}{7}$,二者的含氢量不同,不符合题意,故A错误;
B.丙烷的分子式为C3H8,氢元素的质量分数为:$\frac{8}{44}$=$\frac{2}{11}$,乙醛的分子式为C2H4O,氢元素的质量分数为:$\frac{4}{44}$=$\frac{1}{11}$,二者的含氢量不同,不符合题意,故B错误;
C.乙烯分子中含氢量为:$\frac{4}{28}$=$\frac{1}{7}$,乙酸乙酯的分子式为:C4H8O2,最简式为C2H4O,其含氢量为:$\frac{4}{44}$=$\frac{1}{11}$,二者的含氢量不同,故C错误;
D.甲醛的分子式为CH2O,葡萄糖的分子式为C6H12O6,其最简式为CH2O,所以二者的含氢量相同,符合题意,故D正确;
故选D.
点评 本题考查混合物的计算,难度中等,根据题干信息得出混合物分子中含氢量相等是解题的关键,试题侧重考查学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 | 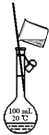 | 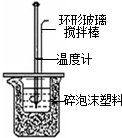 | 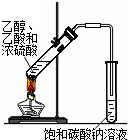 |
| A.实验室制取氨气 | B.配制100mL 0.1mol/L盐酸 | C.测定中和反应 的反应热 | D.实验室制备 乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MoS2煅烧产生的尾气可直接排到空气中 | |
| B. | MoO3不溶于氢氧化钠溶液 | |
| C. | H2MoO4是一种强酸 | |
| D. | 利用H2、CO和Al分别还原等量的MoO3,消耗还原剂的物质的量之比为3:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含硫酸的废液倒入水槽,用水冲入下水道 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 温度计不慎打破,散落的水银应用硫粉处理后收集 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H6 | C. | C3H6 | D. | C3H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
| 分装日期 | |
| 分装企业 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com