
| A、FeCl2 |
| B、Na2SO3 |
| C、NaOH |
| D、AlCl3 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、2Na218O2+2H2O=4Na18OH+O2↑ |
| B、2KMnO4+5H218O2+3H2SO4=K2SO4+2MnSO4+518O2↑+8H2O |
| C、NH3?2H2O+HCl=NH4Cl+2H2O |
| D、K37ClO3+6HCl=K37Cl+3Cl2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、装置(I)用于I2与NH4Cl混合物的分离 |
| B、装置(Ⅱ)用于制取少量纯净的CO2气体 |
| C、装置(Ⅲ)用于去除Fe(0H)3胶体中含有的可溶性物质 |
| D、装置(Ⅳ)用于HC1的吸收,以防倒吸 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、四种毒品中都含有苯环,都属于芳香烃 |
| B、摇头丸经过消去反应、加成反应可制取冰毒 |
| C、用酸性高锰酸钾溶液可以鉴别大麻和摇头丸 |
| D、氯胺酮分子中环上所有碳原子可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
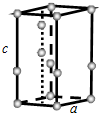
查看答案和解析>>
科目:高中化学 来源: 题型:
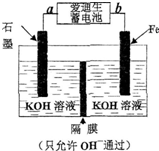 铁及其化合物均为重要化合物.回答下列问题
铁及其化合物均为重要化合物.回答下列问题| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/m01 | 1.0 | 1.5 | 1.0 | 1.0 |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 硫酸 化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g?cm-3 质量分数:98% |
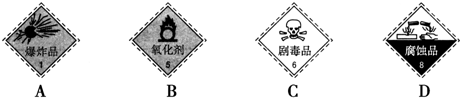
查看答案和解析>>
科目:高中化学 来源: 题型:
 用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积).
用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用待测液润洗滴定用的锥形瓶 |
| B、滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
| C、玻璃棒蘸取溶液滴到放在表面皿上的pH试纸上 |
| D、Na2CO3溶液保存在带玻璃塞的试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com