
已知两个热化学方程式:
C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol;
2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol.
现有0.2mol炭粉和H2组成悬浮气,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是()
A. 1:1 B. 1:2 C. 2:3 D. 3:2
考点: 有关反应热的计算.
专题: 化学反应中的能量变化.
分析: 根据物质的量与反应放出的热量成正比,利用热化学反应方程式计算C、H2燃烧放出的热量,以此来计算.
解答: 解:设碳粉xmol,则氢气为(0.2﹣x)mol,则
C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol
1 393.5kJ
x 393.5xkJ
2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol
2 483.6kJ
(0.2﹣x)mol 241.8(0.2﹣x)kJ
所以393.5xkJ+241.8(0.2﹣x)kJ=63.53kJ,
解得x=0.1mol,
则炭粉与H2的物质的量之比为0.1mol:0.1mol=1:1,
故选A.
点评: 本题考查有关反应热的计算,明确热化学反应方程式中物质的量与热量的关系即可解答,题目难度不大.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:
一定条件下存在反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol CO和1mol H2O,在Ⅱ中充入1mol CO2和1mol H2,在Ⅲ中充入2mol CO和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是()
A. 容器Ⅰ、Ⅱ中正反应速率相同
B. 容器Ⅰ、Ⅲ中反应的平衡常数相同
C. 容器Ⅰ中CO的物质的量比容器Ⅱ中的多
D. 容器Ⅰ中CO的物质的量比容器Ⅱ中的少
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是()
A. 热化学方程式各物质前的化学计量数不表示分子个数只代表物质的量
B. 热化学方程式未注明温度和压强时,△H表示标准状况下的数据
C. 同一化学反应,化学计量数不同,△H不同,化学计量数相同而状态不同,△H也不相同
D. 化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比
查看答案和解析>>
科目:高中化学 来源: 题型:
在100g碳不完全燃烧所得气体中,CO占1/3体积,CO2占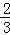 体积,且:
体积,且:
C(s)+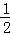 O2(g)═CO(g)△H=﹣110.35kJ;
O2(g)═CO(g)△H=﹣110.35kJ;
CO(g)+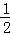 O2(g)═CO2(g)△H=﹣282.5kJ
O2(g)═CO2(g)△H=﹣282.5kJ
与这些碳完全燃烧相比,损失的热量是()
A. 392.92 kJ B. 2489.4 kJ C. 784.72 kJ D. 3274.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
由金红石(TiO2)制取单质Ti,涉及到的步骤为:TiO2→TiCl4 Ti已知:①C(s)+O2(g)=CO2(g);△H=﹣393.5kJ•mol﹣1②2CO(g)+O2(g)=2CO2(g);△H=﹣566kJ•mol﹣1③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);△H=+141kJ•mol﹣1,则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H= kJ/mol.
Ti已知:①C(s)+O2(g)=CO2(g);△H=﹣393.5kJ•mol﹣1②2CO(g)+O2(g)=2CO2(g);△H=﹣566kJ•mol﹣1③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);△H=+141kJ•mol﹣1,则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H= kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
若在铜片上镀银时,下列叙述正确的是()
①将铜片接在电源的正极上
②将银片接在电源的正极上
③在铜片上发生的反应是:Ag++e﹣→Ag
④在银片上发生的反应是:4OH﹣﹣4e﹣→O2↑+2H2O
⑤需用硫酸铜溶液为电镀液
⑥需用硝酸银溶液为电镀液.
A. ①③⑥ B. ②③⑥ C. ①④⑤ D. ②③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
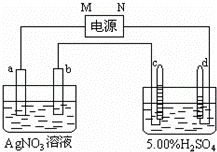
图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.回答:
(1)直流电源中,M为 极.
(2)Pt电极上生成的物质是银,其质量为 g.
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为:2: : :1.
(4)AgNO3溶液的浓度(填增大、减小或不变.下同) ,AgNO3溶液的pH ,H2SO4溶液的浓度 ,H2SO4溶液的pH .
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液的质量为 g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com