
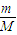 计算20g氢氧化钠的物质的量,根据c=
计算20g氢氧化钠的物质的量,根据c=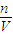 计算氢氧化钠溶液物质的量浓度;溶液是均匀的取出的5ml氢氧化钠溶液及剩余的溶液浓度与原氢氧化钠溶液浓度相同;根据n=cV计算5ml溶液中氢氧化钠的物质的量,再根据m=nM计算5ml溶液中氢氧化钠的质量.
计算氢氧化钠溶液物质的量浓度;溶液是均匀的取出的5ml氢氧化钠溶液及剩余的溶液浓度与原氢氧化钠溶液浓度相同;根据n=cV计算5ml溶液中氢氧化钠的物质的量,再根据m=nM计算5ml溶液中氢氧化钠的质量.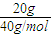 =0.5mol,
=0.5mol,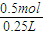 =2mol/L.
=2mol/L.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com