
 .
.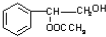 或
或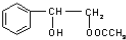 .
. .
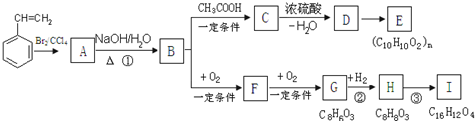
. 分析 苯乙烯与溴发生加成反应生成A为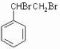 ,A发生水解生成B为
,A发生水解生成B为 ,B与乙酸发生酯化反应生成C,C发生消去反应脱水生成D,故C
,B与乙酸发生酯化反应生成C,C发生消去反应脱水生成D,故C 或
或 ,D对应为
,D对应为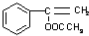 或
或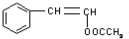 ,D加聚得到E.B中含有羟基,可以被氧化生成F为
,D加聚得到E.B中含有羟基,可以被氧化生成F为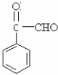 ,F继续氧化生成G,则G为
,F继续氧化生成G,则G为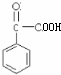 ,根据H和I的分子式可以判断,反应③是2分子H脱去2分子水形成环酯,故H为
,根据H和I的分子式可以判断,反应③是2分子H脱去2分子水形成环酯,故H为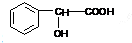 ,I为
,I为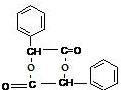 ,据此解答.
,据此解答.
解答 解:苯乙烯与溴发生加成反应生成A为 ,A发生水解生成B为
,A发生水解生成B为 ,B与乙酸发生酯化反应生成C,C发生消去反应脱水生成D,故C
,B与乙酸发生酯化反应生成C,C发生消去反应脱水生成D,故C 或
或 ,D对应为
,D对应为 或
或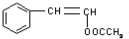 ,D加聚得到E.B中含有羟基,可以被氧化生成F为
,D加聚得到E.B中含有羟基,可以被氧化生成F为 ,F继续氧化生成G,则G为
,F继续氧化生成G,则G为 ,根据H和I的分子式可以判断,反应③是2分子H脱去2分子水形成环酯,故H为
,根据H和I的分子式可以判断,反应③是2分子H脱去2分子水形成环酯,故H为 ,I为
,I为 .
.
(1)一定条件下,苯乙烯发生聚合反应生成聚苯乙烯,反应方程式为: ,
,
故答案为: ;
;
(2)C中分子内脱1分子水生成D,所以由C生成D发生的是消去反应,
故答案为:消去反应;
(3)通过以上分析知,C的结构简式可能为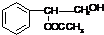 或
或 ,
,
故答案为: 或
或 ;
;
(4)H有多种同分异构体,同时符合:与FeCl3溶液发生显色反应,说明该物质含有酚羟基,苯环上只有两个取代基,酚羟基是1个,1molH最多能与3molNaOH反应,另外基团满足与氢氧化钠消耗2mol氢氧化钠,为则取代基为-OOCCH3,该取代基与酚羟基由邻、间、对三种位置关系,所以有三种同分异构体,
故答案为:3种;
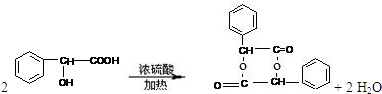
(5)通过以上分析知,反应③的化学方程式是: ,
,
故答案为: .
.
点评 本题考查有机推断与合成,是对有机化合物知识的综合考查,能较好的考查考生的阅读、自学能力和思维能力,有机推断几乎是高考不变的一个题型,每年高考中必考,是高考热点题型,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 4、5 | B. | 5、4 | C. | 3、4 | D. | 5、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液(NaHCO3),加入适量的NaOH溶液 | |
| B. | Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液后过滤 | |
| C. | NaHCO3溶液(Na2CO3),通入过量的CO2气体 | |
| D. | Na2O2粉末(Na2O),将混合物在空气中加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含有1个双键的直链有机物 | B. | 含有2个双键的直链有机物 | ||
| C. | 含有1个双键的环状有机物 | D. | 含有1个叁键的直链有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
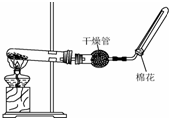 A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{+X}{→}$B$\stackrel{+X}{→}$C
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{+X}{→}$B$\stackrel{+X}{→}$C查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mo1 C2H4 | B. | 11.2L(标准状况) C2H2 气体 | ||
| C. | 23g Na | D. | 9g H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20g | B. | 25.4g | C. | 31.6g | D. | 34.8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com