
| A. | NO3- | B. | Cl- | C. | Br- | D. | CO32- |
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与铁反应时分别生成硫化亚铁和氯化铁 | |
| B. | 与氢气反应的条件分别是加热和点燃(或光照) | |
| C. | 硫化氢的溶解度比氯化氢小得多 | |
| D. | 氯气能从氢硫酸中置换出单质硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{92}^{235}U$原子核中含有92个中子 | |
| B. | ${\;}_{92}^{235}U$原子核外有92个电子 | |
| C. | ${\;}_{92}^{235}U$与${\;}_{92}^{238}U$互为同素异形体 | |
| D. | ${\;}_{92}^{235}U$与${\;}_{92}^{238}U$物理性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用胶状氢氧化铝凝聚水中的悬浮物进行净水 | |
| B. | 用红棕色氧化铁制造红色油漆 | |
| C. | 氢氧化铝作为医用的胃酸中和剂 | |
| D. | 用氧化铝制造耐火坩埚和耐火管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成44.8LN2 | |
| B. | 有0.250molKNO3被氧化 | |
| C. | 转移电子的物质的量为1.25mol | |
| D. | 被氧化的N原子的物质的量为3.00mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
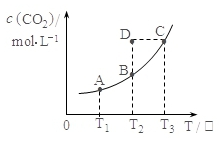 在密闭容器中存在下列平衡:CO(g)+H 2O(g)?CO2(g)+H 2(g);CO 2(g)的平衡物质的量浓度c(CO 2)与温度T的关系如图所示.下列说法错误的是( )
在密闭容器中存在下列平衡:CO(g)+H 2O(g)?CO2(g)+H 2(g);CO 2(g)的平衡物质的量浓度c(CO 2)与温度T的关系如图所示.下列说法错误的是( )| A. | 平衡状态A与C相比,平衡状态A的c(CO)小 | |
| B. | 在T 2时,若反应处于状态D,则一定有V 正<V 逆 | |
| C. | 反应CO(g)+H 2O(g)?CO 2(g)+H 2(g) 的△H>0 | |
| D. | 若T 1、T 2时的平衡常数分别为K 1、K 2,则K 1<K 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com