
����Ŀ��X��Y��Z��Q��E����Ԫ���У�Xԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�Yԭ�Ӻ����L���������K���������Z�ǵؿ��ں�����������������ߵ�Ԫ�أ�Q�ĺ˵������X��Z�ĺ˵����֮�ͣ�E��Ԫ�����ڱ��ĸ�Ԫ���е縺�������ش��������⣺
��1��X��ԭ�ӽṹʾ��ͼΪ��Y�ļ۵��ӹ����ʾʽΪ ��
��2��XZ2��YZ2���ӵ�����ṹ�ֱ����� �� ��ͬ������������ˮ�е��ܽ�Ƚϴ������д����ʽ���������� ��
��3��Q��Ԫ�ط����� �� �����ڵ������壬���ĺ�������Ų�ʽΪ �� ���γɻ�����ʱ��������ϼ�Ϊ
��4���������ʾʽд��E���⻯��ˮ��Һ�д��ڵ�������� ��
���𰸡�
��1��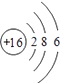 ��
��![]()
��2��V�Σ�ֱ���Σ�SO2��SO2�Ǽ��Է��ӣ�H2OҲ�Ǽ��Է��ӣ��������ܣ���CO2�ǷǼ��Է���
��3��Cr���ģ���B��1s22s22p63s23p63d54s1��+6
��4��F��H��F��F��H��O��O��H��F��O��H��O
���������⣺Xԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ���������Ų�ӦΪ1s22s22p63s23p4 �� ΪSԪ�أ�Yԭ�Ӻ����L���������K���������Y��2�����Ӳ㣬����������Ϊ4����YΪCԪ�أ�Z�ǵؿ��ں�����ߵ�Ԫ�أ�ΪOԪ�أ�Q�ĺ˵������X��Z�ĺ˵����֮�ͣ�ԭ������Ϊ24��ΪCrԪ�أ�E��Ԫ�����ڱ��ĸ�Ԫ���е縺�����ӦΪFԪ�أ���1�������Ϸ�����֪��XΪS����ԭ�ӽṹʾ��ͼΪΪ 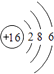 ��YΪC���۵����Ų�Ϊ2s22p2 �� �۵��ӹ����ʾΪ
��YΪC���۵����Ų�Ϊ2s22p2 �� �۵��ӹ����ʾΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� 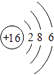 ��
�� ![]() ����2��SO2�У�S��O�γ�2���ļ�����1���µ��Ӷԣ�ΪV�Σ�CO2�У�C��O�γ�2���ļ���û�йµ��Ӷԣ�Ϊֱ���Σ�SO2�Ǽ��Է��ӣ�H2OҲ�Ǽ��Է��ӣ��������ܣ���CO2�ǷǼ��Է��ӣ���SO2��ˮ���ܽ�ȸ���
����2��SO2�У�S��O�γ�2���ļ�����1���µ��Ӷԣ�ΪV�Σ�CO2�У�C��O�γ�2���ļ���û�йµ��Ӷԣ�Ϊֱ���Σ�SO2�Ǽ��Է��ӣ�H2OҲ�Ǽ��Է��ӣ��������ܣ���CO2�ǷǼ��Է��ӣ���SO2��ˮ���ܽ�ȸ���
���Դ��ǣ�V�Σ�ֱ���Σ�SO2��SO2�Ǽ��Է��ӣ�H2OҲ�Ǽ��Է��ӣ��������ܣ���CO2�ǷǼ��Է��ӣ���3��QΪCr��ԭ������Ϊ24��λ�����ڱ��������ڢ�B�壬��������Ų�ʽΪ1s22s22p63s23p63d54s1 �� ����ϼ�Ϊ+6�ۣ�
���Դ��ǣ�Cr���ģ���B��1s22s22p63s23p63d54s1��+6����4��HF��ˮ��Һ�У�F�ĵ縺�Խϴ�����һ���ӵ�HF��ˮ�е�H�γ�������ɱ�ʾΪH��F��H����ԭ�Ӻͷ���������е���ԭ��֮�����γ�������ɱ�ʾΪ F��H��O����ԭ�Ӻ�ˮ�����е���ԭ�����γ�����ɱ�ʾΪO��H��F����ԭ�Ӻ���һ��ˮ�����е���ԭ�����γ�����ɱ�ʾΪO��H��O��
���Դ��ǣ�F��H��F��F��H��O��O��H��F��O��H��O��


 ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д� ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Na2CO3��NaHCO3���ʵıȽ��У���ȷ���ǣ� ��
A.��Ũ�ȵ���Һ�е���ϡ���ᣬ�ų�����Ŀ���Na2CO3<NaHCO3
B.���ȶ���Na2CO3<NaHCO3
C.����ʱˮ����Na2CO3<NaHCO3
D.��Է�������Na2CO3<NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������� ![]() ����ҩ���ƹ����з��ֵ�һ����Ҫ�������ʣ����п����ʡ���������������ȱѪ�����ʣ�������ij�о�С�������һ��������
����ҩ���ƹ����з��ֵ�һ����Ҫ�������ʣ����п����ʡ���������������ȱѪ�����ʣ�������ij�о�С�������һ�������� ![]() �����H�ĺϳ�·�ߣ�
�����H�ĺϳ�·�ߣ� 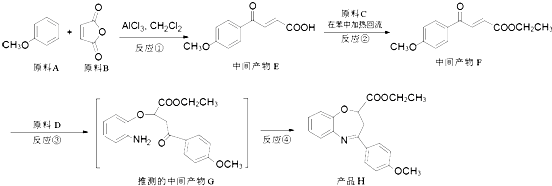
��1��ԭ��A��ͬ���칹���У����б������Һ˴Ź�����������4���������д����ṹ��ʽ����
��2����Ӧ�ڵĻ�ѧ����ʽ�� ��
��3���۵ķ�Ӧ������ �� ԭ��D�к��еĹ������������� ��
��4��ԭ��B�������������������������ᣨ˳��ϩ��� ![]() ���������������Ծ����б仯�ֱ�õ�ƻ���ᣨ
���������������Ծ����б仯�ֱ�õ�ƻ���ᣨ ![]() ���;ۺ���Q��
���;ۺ���Q�� 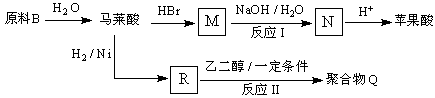
д����Ӧ��ͷ�Ӧ��Ļ�ѧ����ʽ���� ��
��5�����������������м����F��ͬ���칹����Ŀ���������������칹����д����������һ�ֵĽṹ��ʽ �� ��i���ܷ���������Ӧ��
��ii�������к�����ȡ���ı����ṹ����������ȡ�����ǣ���COOCH3�� ![]() ���Ҷ��ߴ��ڶ�λ��
���Ҷ��ߴ��ڶ�λ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���������װ�õ���������ȷ���ǣ� �� 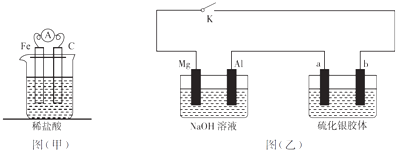
A.��װ��Ϊ�������ⸯʴ������������ͭ�����װ�þ���ͭ��������ʴ
B.������װ���еĵ�������Ϊ��Դ�����۵�Դ��ô���ӣ�C�缫�϶���������ų�
C.��װ����K�رպ�a��������ɫ������
D.������װ���е�NaOH��Һ��ΪHCl��Һ����K�رպ�b����ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������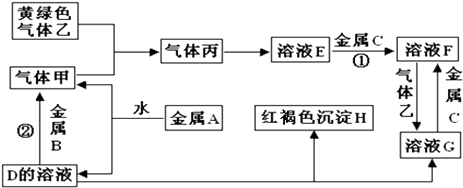
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��A��H�� G������
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��Ӧ����Ӧ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ȼ���г���CaF2����ʽ���ڣ�
��1�����й���CaF2�ı�����ȷ���� ��
a��Ca2+��F��������ھ�����������
b��F�������Ӱ뾶С��Cl�� �� ��CaF2���۵����CaCl2
c���������ӱ�Ϊ2��1�����ʣ�����CaF2���幹����ͬ
d��CaF2�еĻ�ѧ��Ϊ���Ӽ������CaF2������״̬���ܵ���
��2��CaF2������ˮ���������ں�Al3+����Һ�У�ԭ�����������ӷ���ʽ��ʾ����
��֪AlF63������Һ�п��ȶ����ڣ�
��3��F2ͨ��ϡNaOH��Һ�п�����OF2 �� OF2���ӹ���Ϊ �� ������ԭ�ӵ��ӻ���ʽΪ
��4��F2������±�ص��ʷ�Ӧ�����γ�±�ػ��������ClF3��BrF3�ȣ���֪��ӦCl2��g��+3F2��g���T2ClF3��g����H=��313kJmol��1 �� F��F���ļ���Ϊ159kJmol��1 �� Cl��Cl���ļ���Ϊ242kJmol��1 �� ��ClF3��Cl��F����ƽ������ΪkJmol��1 �� ClF3���ۡ��е��BrF3������ߡ��͡�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ǧ���صĹ���ԭ��Ϊ��Pb+PbO2+2H2SO4�T2PbSO4+2H2O���ж�ͼ�������жϲ���ȷ���ǣ� �� 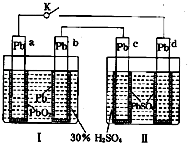
A.K�պ�ʱ��d�缫��Ӧʽ��PbSO4+2H2O��2e��=PbO2+4H++SO42��
B.����·��ת��0.2mol����ʱ��I�����ĵ�H2SO4Ϊ0.2 mol
C.K�պ�ʱ��II��SO42����c�缫Ǩ��
D.K�պ�һ��ʱ���II�ɵ�����Ϊԭ��أ�d�缫Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵͼ��������˵����ȷ����
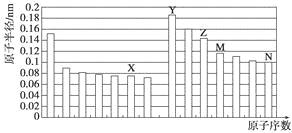
A. Z��N����Ԫ�ص����Ӱ뾶��ȣ�ǰ�߽ϴ�
B. X��N����Ԫ�ص���̬�⻯��ķе���ȣ�ǰ�߽ϵ�
C. ��X��M����Ԫ����ɵĻ����ﲻ�����κ��ᷴӦ��������ǿ�Ӧ
D. Z���������ֱܷ��ܽ���Y�����������N���⻯���ˮ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܼ����ֳ��ܻ�����2011����̨�屻�������ܻ���ʳƷ�Ѵ�961�6��1�������������������棬���ڱ�����������Ҳ��̪�����������ʣ�����ʳƷ�п���Υ�����ӵķ�ʳ�����ʺ������õ�ʳƷ���Ӽ����������й��̾����л��ϳ�ij���ܼ���·�ߣ���֪��������ڸ�����ص������£������ɱ��������Ȼ������磺��ͼ1��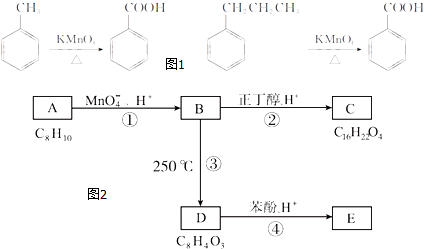
������A��E��ת����ϵ��ͼ2��ʾ����֪��A�Ƿ��㻯���ֻ������3��һ�廯���B�����ԣ�C�dz������ܼ���D���л��ϳɵ���Ҫ�м���ͳ��û�ѧ�Լ���DҲ��������ԭ�ϴ������õ�����E��һ�ֳ��õ�ָʾ����̪��
��1��A�Ļ�ѧ����Ϊ ��
��2��B�Ľṹ��ʽΪ ��
��3����B����C�Ļ�ѧ����ʽΪ �� �÷�Ӧ������Ϊ��Ӧ��
��4��D�Ľṹ��ʽΪ �� ��D���ʵĺ˴Ź�������ͼ�У��������壬�����֮��Ϊ ��
��5��A��ͬ���칹�������ڷ����廯��������֣�����һ�ȴ�����������������д�ṹ��ʽ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com