
 ②
② ③
③ ④
④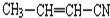
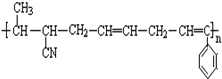 (结构如图所示)的正确组合为( )
(结构如图所示)的正确组合为( )| A、①②④ | B、①②⑤ |
| C、②④⑤ | D、③④⑤ |
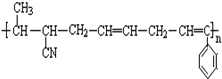 可知,该有机物为加聚反应产物,其主链含有两个碳碳双键,先将中括号去掉,然后从左向右,按照“见双键,四个碳,无双键,两个碳”画线断开:
可知,该有机物为加聚反应产物,其主链含有两个碳碳双键,先将中括号去掉,然后从左向右,按照“见双键,四个碳,无双键,两个碳”画线断开: ,则可以得到该有机物的三种单体:④
,则可以得到该有机物的三种单体:④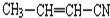 、⑤CH2=CH-CH=CH2、③
、⑤CH2=CH-CH=CH2、③ ,
,

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某实验小组对H2O2的分解做了如下探究:
某实验小组对H2O2的分解做了如下探究:| 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 | |
| 无催化剂 不加热 |
几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂 加热 |
360 | 480 | t | 720 |
| MnO2催化剂 加热 |
10 | 25 | 60 | 120 |
| 催化剂 MnO2 |
操作 情况 |
观察结果 | 反应完成 所需时间 |
| 粉末状 | 混合 不振荡 |
剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30min |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(NH4+)相等的(NH4)2 S04、NH4HS04、NH4Cl溶液中:c(NH4 HS04)>c[(NH4)2S04]>c(NH4Cl) |
| B、已知HF的酸性比CH3 COOH的强,pH相等的NaF与CH3COOK溶液中:c(Na+)-c(F-)<c(K+)-c(CH3COO-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(CH3 COO-)>c(Na+)>c(H+)>c(OH-) |
| D、溶有等物质的量NaClO、NaHC03的溶液中:c(HClO)+c(ClO-)═c( HCO3?)+c(H2CO3 )+2c(CO32?) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com