
| c(H2SO3) |
| c(HSO3-) |
| c(H+)c(HSO3-) |
| c(H2SO3) |
| c(H2SO3)Kw |
| c(HSO3-)c(H+) |
| c(TaI4)c(S2) |
| c2(I2) |
| c(TaI4)c(S2) |
| c2(I2) |
| 0.5x��0.5x |
| (1-x)2 |
| c(TaI4)c(S2) |
| c2(I2) |
| c(H+)c(HSO3-) |
| c(H2SO3) |
| c(H2SO3)Kw |
| c(HSO3-)c(H+) |
| c(H2SO3) |
| c(HSO3-) |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� ʳ | �� �� |
| �� ʳ | ������ |
| �� Ʒ | �� �� |
| ��IJ��� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
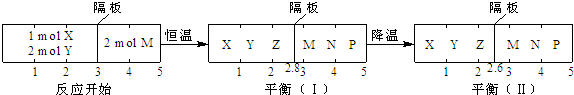
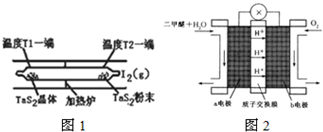
| A����Ӧ�ٵ��淴Ӧ�Ƿ��ȷ�Ӧ | ||
| B����ƽ�⣨��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ11��10 | ||
C����ƽ�⣨��ʱ��X��ת����Ϊ
| ||
| D����ƽ�⣨��ƽ�⣨���У�M������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
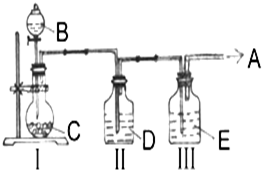 ʵ��������ȡ�������﴿��������A��������ͼװ��
ʵ��������ȡ�������﴿��������A��������ͼװ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
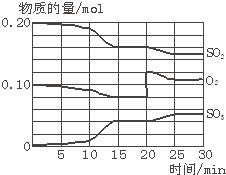
| A��Cu2S���������������ǻ�ԭ���� |
| B��5 mol FeS2������Ӧ����14mol����ת�� |
| C�������е�SO42-��һ�������������� |
| D��FeS2ֻ����ԭ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com