
【题目】SiO2晶体的部分结构如图所示,关于该晶体下列说法错误的是( )

A.Si原子杂化类型为sp3
B.Si、O的原子个数比为1:4
C.Si原子数目与Si—O键数目比为1:4
D.SiO2晶体中最小环为12元环
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)在食品加工、印染、印刷、制革以及有机合成等工业中应用广泛。实验室模拟工业湿法制备焦亚硫酸钠装置如图所示。
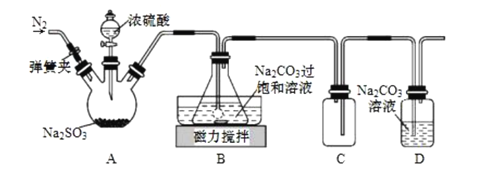
打开弹簧夹,通入一段时间N2后关闭弹簧夹,加入一定量浓硫酸;不断搅拌,控制反应温度在40℃左右,当溶液pH约为4.1时,停止反应,降温至20℃左右静置结晶。
已知:
①温度在40℃左右时,发生反应2NaHSO3=Na2S2O5+H2O。
②温度过高时焦亚硫酸钠分解:Na2S2O5=Na2SO3+SO2↑。
③焦亚硫酸钠与水易发生反应:Na2S2O5+H2O=2NaHSO3。
回答下列问题:
(1)A装置中所加硫酸通常为1:1(体积比)的浓硫酸,一般不采用90%以上的浓硫酸,原因是__。
(2)B装置中控制反应温度40℃在左右的方法是__;锥形瓶中生成NaHSO3的离子方程式为__。
(3)装置C的作用是__。
(4)锥形瓶中析出固体经减压抽滤、洗涤、晾干,可获产品。洗涤操作中依次用饱和SO2水溶液、无水乙醇洗涤,其作用是__。
(5)反应结束后,需要再次打开弹簧夹,通入一段时间N2,目的是__。
(6)某同学认为Na2S2O5属于强碱弱酸盐,在溶液中水解显碱性。实际他测得Na2S2O5溶液显酸性,请用数据帮他分析溶液显酸性的原因__。
(已知:常温下H2SO3电离常数Ka1=1.54×10-2,Ka2=1.02×10-7)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯: 6 H2(g) +2CO2(g)![]() CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
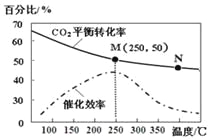
A. 生成乙烯的速率:v(M)一定小于v(N)
B. 化学平衡常数:KN>K M
C. 当温度高于250℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低
D. 若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物K是治疗急、慢性支气管炎及支气管扩张、肺气肿、肺结核等疾病药物的中间体,其合成路线如下,回答下列问题:

已知信息:
①
②![]()
③ R1CHO+R2NH2 ![]() R1CH=NR2
R1CH=NR2
(1)A的名称为_______,G的结构简式为_____,F→G的反应类型为___,H中官能团的名称为___________。
(2)D→E的反应方程式为______。
(3)写出化合物D同时符合下列条件的同分异构体的结构简式______。
①苯环上有两个取代基,官能团与D相同,苯环上的一氯代物有两种
②核磁共振氢谱显示峰面积比为2:2:2:3
(4)已知:通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。写出以![]() 和
和![]() 为原料制备
为原料制备 的合成路线 __(其他试剂任选)。
的合成路线 __(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸亚铁((C6H11O7)2Fe)是常用的补铁剂,易溶于水,几乎不溶于乙醇。葡萄糖酸亚铁的制备方法之一是由新制备的碳酸亚铁(白色固体,微溶于水)与葡萄糖酸反应而制得,其流程如下:
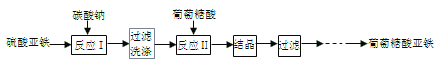
(1)用下图装置制备FeCO3
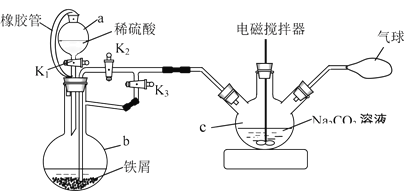
①仪器b的名称为_________。仪器a中橡胶管的作用是_______。
②反应开始时,先打开活塞K1和K3,关闭K2,目的是_______。一段时间后,关闭_______,打开______,目的是_______。
③将制得的FeCO3过滤、洗涤。检验沉淀已经洗涤干净的试剂为______(若多种试剂,按试剂使用由先到后的顺序填写)。
④用NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时有气体产生,反应的离子方程式为________。
(2)反应II中加入过量葡萄糖酸使溶液显弱酸性,原因是________。
(3)葡萄糖酸亚铁结晶时需加入乙醇,目的是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用氯酸钠(NaClO3)为原料制取,(常温下ClO2为气态),下列说法错误的是
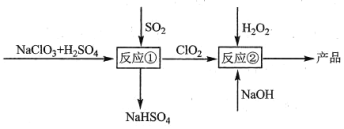
A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1
B.反应①后生成的气体要净化后进入反应②装置
C.升高温度,有利于反应②提高产率
D.反应②中有气体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素为地壳中含量最高的元素,可形成多种重要的单质和化合物。
(1)氧元素位于元素周期表中_____区;第二周期元素中,第一电离能比氧大的有_____种。
(2)O3可用于消毒。O3的中心原子的杂化形式为_____;其分子的VSEPR模型为_____,与其互为等电子体的离子为_____(写出一种即可)。
(3)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释C2H5OH的沸点高于CH3OCH3的原因为_____。
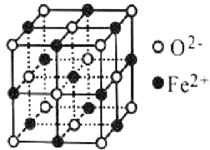
(4)氧元素可与Fe形成低价态氧化物FeO。FeO立方晶胞结构如图所示,则Fe2+的配位数为_____;与O2-紧邻的所有Fe2+构成的几何构型为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中( )
A.至少存在3种离子
B.Cl-一定存在,且c(Cl)≥0.4mol/L
C.SO42-、NH4+、一定存在,Cl-可能不存在
D.CO32-、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li、Fe、As均为重要的合金材料,NA为阿伏加德罗常数的值。回答下列问题:
(1)基态Li原子核外电子占据的空间运动状态有________个,占据最高能层电子的电子云轮廓图形状为_________。
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为_________。
(3)基态Fe3+比基态Fe2+稳定的原因为____________。
(4)KSCN和K4[Fe(CN)6]均可用于检验Fe3+。
①SCN-的立体构型为_______,碳原子的杂化方式为_____________。
②K4[Fe(CN)6]中所含元素的第一电离能由大到小的顺序为__________(用元素符号表示);1 mol [Fe(CN)6]4-中含有σ键的数目为____________。
(5)H3AsO3的酸性弱于H3AsO4的原因为____________________。
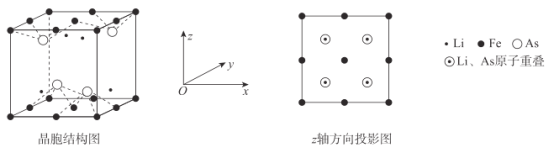
(6)Li、Fe和As可组成一种新型材料,其立方晶胞结构如图所示。若晶胞参数为a nm,阿伏加德罗常数的值为NA,则该晶体的密度可表示为______g●cm-3。(列式即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com