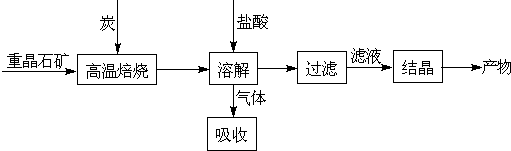
某研究小组在实验室中以铜粉(含铁粉5%以上)为原料制取胆矾(CuSO
4?5H
2O)并检测其纯度.本题限选试剂:3mol?L
-1 H
2SO
4、浓硝酸、3%H
2O
2、0.2mol?L
-1 NaOH、20% KSCN.有关物质溶解度如下表(单位:g/100gH
2O).
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
| CuSO4 |
14.3 |
20.7 |
28.5 |
40.0 |
55.0 |
75.4 |
| Cu(NO3)2 |
81.8 |
124.8 |
163.1 |
181.8 |
207.8 |
247.3 |
(1)在答题卡上补充完成制取胆矾的实验方案.
| 实验步骤 |
预期现象 |
| 步骤1:除铁.将铜粉置于烧杯中, . |
|
| 步骤2:溶解.将步骤1得到的铜粉置于烧杯中, . |
|
| 步骤3:结晶.将步骤2所得溶液蒸发浓缩至液面有晶膜出现,冷却至室温,过滤得粗产品. |
/ |
(2)完成步骤1后,检验铜粉中的铁是否除净的实验操作是
.
(3)若胆矾中若含有少量Cu(NO
3)
2?3H
2O,测定其中CuSO
4?5H
2O的含量,实验步骤如下:称量胆矾样品的质量为m
1,加水溶解,滴加足量BaCl
2溶液,充分反应后过滤,将滤渣烘干、冷却,称得其质量为m
2.样品中CuSO
4?5H
2O的质量分数为
(列出算式.化学式量:CuSO
4-160;CuSO
4?5H
2O-250;Cu(NO
3)
2?3H
2O-242;BaSO
4-233)



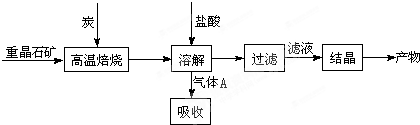
 (2007?淄博三模)铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸.某化学研究小组在实验室中按下列步骤模拟该生产过程.填写下列空白:
(2007?淄博三模)铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸.某化学研究小组在实验室中按下列步骤模拟该生产过程.填写下列空白: 对金属表面进行处理,形成一层致密的氧化物保护膜,是非常有效的一种金属防腐技术.
对金属表面进行处理,形成一层致密的氧化物保护膜,是非常有效的一种金属防腐技术.