
元素周期表是化学学习和科学研究的重要工具,下列对于元素周期表的使用方法不正确的是( )
|
| A. | 为新元素的发现及预测它们的原子结构和性质提供线索 |
|
| B. | 利用元素周期表发现元素的种类和原子的种类相同 |
|
| C. | 在周期表中金属与非金属的分界处,可寻找半导体材料 |
|
| D. | 指导人们在过渡元素中寻找催化剂和耐高温.耐腐蚀的合金材料 |
考点:
元素周期表的结构及其应用.
分析:
A.结合同周期、同族元素性质的相似性、递变性解答;
B.元素是质子数相同、中子数不同的一类原子总称,原子种类远多于元素种类;
C.处于金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性;
B.在过渡元素中寻找制造催化剂元素及制造高温、耐腐蚀合金材料.
解答:
解:A.同周期、同族元素性质具有一定相似性、递变性,位置靠近的元素性质相似,为新元素的发现和预测它们的原子结构和性质提供线索,故A正确;
B.元素是质子数相同、中子数不同的一类原子总称,同一种元素可能有不同核素,所以原子种类远多于元素种类,故B错误;
C.在金属元素和非金属元素交界区域的元素通常既具有金属性又具有非金属性,可以在此寻找良好的半导体材料,如硅等,故C正确;
D.优良的催化剂和耐高温、耐腐蚀的合金材料(如制造火箭、飞机的钛、钼等元素)大多属于过渡元素,故D正确,
故选B.
点评:
本题考查元素周期表与元素周期律的应用,题目较为简单,注意基础知识的积累.


科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒用作引流的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
|
| A. | ①和② | B. | ①和③ | C. | ③和④ | D. | ①和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0,下列研究目的和示意图相符的是()
A B C D
研究目的 压强对反应的影响
(p2>p1) 温度对反应的影响 平衡体系增加O2的浓度对反应的影响 体积恒定的密闭容器中催化剂对反应的影响
图示 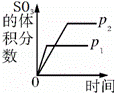
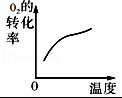
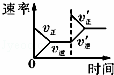

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的性质随着元素原子序数的递增而呈周期性变化的原因是( )
|
| A. | 元素原子的核外电子排布呈周期性变化 |
|
| B. | 元素的原子半径呈周期性变化 |
|
| C. | 元素的化合价呈周期性变化 |
|
| D. | 元素的金属性、非金属性呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中,同主族元素从上到下,原子半径逐渐 (填“增大”或“减小”),元素的金属性逐渐 (填“增强”或“减弱”),非金属性逐渐 (填“增强”或“减弱”);同周期从左到右,原子半径逐渐 (填“增大”或“减小”),元素的金属性逐渐 (填“增强”或“减弱”),非金属性逐渐 (填“增强”或“减弱”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是()
A. 在稀溶液中,1mol酸和1mol碱完全反应所放出的热量,叫做中和热
B. 热化学方程式中,各物质前的化学计量数不表示分子个数
C. 在101kPa时,1mol物质燃烧时所放出的热量叫做该物质的燃烧热
D. 如果反应物所具有的总能量小于生成物所具有的总能量,则反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的密闭容器中,当下列物理量不再变化时,表明A(s)+2B(g)⇌C(g)+D(g)已达平衡的是()
A. 混合气体的压强 B. 混合气体的密度
C. 混合气体的分子数目 D. 混合气体的总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实与氢键有关的是( )
A. 水加热到很高的温度都难以分解
B. 水结冰成体积膨胀,密度减少
C. CH4、SiH4、GeH4、SnH4熔点随相对分子质量增加而升高
D. HF、HCI、HBr、HI的热稳定性依次减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com