
 .
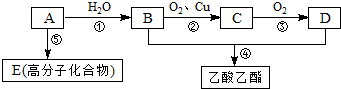
.分析 A是石油裂解气的主要成分,A的产量通常衡量一个国家的石油化工水平,则A为C2H4;A与水发生加成反应得到B为CH3CH2OH,B能氧化得到C为CH3CHO,C氧化得到D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯,乙烯中含有碳碳双键,在一定条件下发生加聚反应生成E为 ,以此解答该题.
,以此解答该题.
解答 解:A是石油裂解气的主要成分,A的产量通常衡量一个国家的石油化工水平,则A为C2H4;A与水发生加成反应得到B为CH3CH2OH,B能氧化得到C为CH3CHO,C氧化得到D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯,乙烯中含有碳碳双键,在一定条件下发生加聚反应生成E为 .
.
(1)A为C2H4,结构式为:

(2)B为CH3CH2OH,含有官能团为羟基,D为CH3COOH,含有官能团为羧基,故答案为:羟基;羧基;
(3)反应①的化学方程式为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,属于加成反应;
反应②的化学方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+H2O,反应类型为氧化反应;
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,加成反应;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+H2O,氧化反应.
点评 本题考查有机物推断,为高频考点,侧重于学生的分析能力的考查,涉及烯烃、醇、醛、羧酸的性质与转化,比较基础,侧重对基础知识的巩固.


科目:高中化学 来源: 题型:选择题
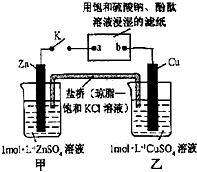
| A. | Cu电极上发生还原反应 | B. | 电子沿Zn→a→b→Cu路径流动 | ||
| C. | 片刻后甲池中c(SO42-)增大 | D. | 片刻后可观察到滤纸b点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
周期 主族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 二 | ① | ② | ③ | ④ | |||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C30H50 | B. | C30H56 | C. | C36H72 | D. | C30H60 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F-离子结构示意图: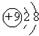 | |
| B. | 氯化钠的电子式: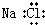 | |
| C. | 二氧化碳的结构式:O=C=O | |
| D. | 碳酸氢钠的电离方程式:NaHCO3=Na++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
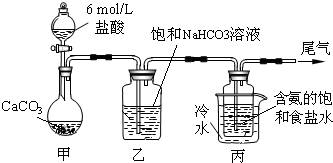
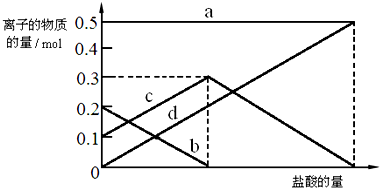
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
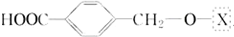 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生. .
. (其中两种).
(其中两种). 为主要原料制备
为主要原料制备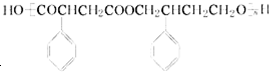 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com