
| A. | 0.10mol∕L Ag+ | B. | 0.20mol∕L Cu2+ | C. | 0.20mol∕L Zn2+ | D. | 0.20mol∕LPb2+ |
分析 在电解池中,阴极上阳离子的放电顺序是:银离子>铜离子>氢离子,只有放电顺序在H+前的才析出金属,根据电极反应结合电子守恒来计算即可.
解答 解:Zn2+和Pb2+的放电顺序都在H+后面,所以含有这两种阳离子的盐溶液中,阴极上放出H2,而含有银离子和铜离子这两种阳离子的盐溶液中,Ag和Cu金属先在阴极析出.
A、0.10mol∕LAg+在氢离子之前放电,金属银的质量是 0.1mol/L×0.1L×108g/mol=1.08g;
B、铜离子先放电,100mL0.20mol∕LCu2+就会得到0.04mol电子,所以析出金属铜的质量为$\frac{1}{2}$×0.04mol×64g/mol=1.28g;
C、Zn2+的放电顺序在H+后面,所以含有这种阳离子的盐溶液中,阴极上放出H2,不会析出金属;
D、Pb2+的放电顺序在H+后面,所以含有这种阳离子的盐溶液中,阴极上放出H2,不会析出金属.
所以析出金属质量最大的是0.20mol∕LCu2+.
故选B.
点评 本题考查学生电解池上阴极上离子的放电顺序并结合电子守恒来计算析出金属的质量,综合性较强,题目难度中等.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:解答题
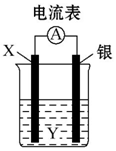 依据2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题:
依据2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:ClO-+CO2+H2O=HClO+HCO3- | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ | |
| C. | 从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- | |
| D. | Ca(ClO)2溶液中通入过量的SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y既可是金属也可是非金属 | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | X、Z形成的某化合物在熔融状态下不导电 | |
| D. | WY2分子中既有非极性键又有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以共存 | |
| B. | 水电离的c(H+)=1×10-3mol/L的溶液中:Na+、Fe3+、SO42-、Cl- | |
| C. | 由0.l moI/L BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH- | |
| D. | $\frac{{K}_{W}}{(O{H}^{-})}$=1×10-13mol/L 的溶液中:Ba2+、ClO-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaCl溶液中滴入AgNO3溶液有沉淀 | |
| B. | 同一钢笔同时使用不同牌号的墨水易发生堵塞 | |
| C. | 在河流入海口易形成三角洲 | |
| D. | 在实验中不慎手被玻璃划破,可用FeCl3溶液应急止血 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
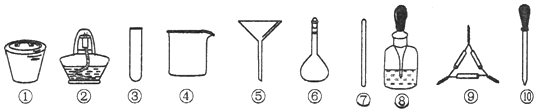
| A. | 将海带剪碎后灼烧成灰,选用①、②和⑨ | |
| B. | 将海带灰加蒸馏水溶解,选用④、⑥和⑦ | |
| C. | 过滤得到滤液,选用④、⑤和⑦ | |
| D. | 取滤液,先加入几滴稀硫酸,再滴加H2O2,最后滴加淀粉溶液,选用③和⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c1=2c2 | B. | c2=2cl | C. | c2>2c1 | D. | c2<2cl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com