
����Ŀ������������Ԫ��V��W��X��Y��Z��ԭ����������������������Ԫ����ɵľ��������У�n��r��u�����嵥�ʣ������Ϊ�����n�ǻ���ɫ���壬m����ʹʪ��ĺ�ɫʯ����ֽ��������ɫ���壬p����ɫҺ�壬q�ǵ���ɫ���塣���ǵ�ת����ϵ��ͼ��ʾ��
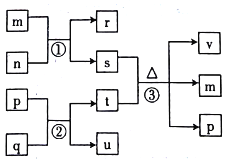
����˵����ȷ����
A. ʵ������ȡm��uʱ�����巢��װ�ÿ�����ͬ
B. ԭ�Ӱ뾶��W>X>Y
C. ��Ӧ�����ھ�Ϊ�û���Ӧ
D. n��t��Һ��Ӧʱ��t����ԭ��
���𰸡�A
��������n��r��u�����嵥�ʣ������Ϊ�����n�ǻ���ɫ���壬ӦΪ������m����ʹʪ��ĺ�ɫʯ����ֽ��������ɫ���壬ӦΪNH3��p����ɫҺ�壬ӦΪˮ��q�ǵ���ɫ���壬ӦΪNa2O2����Na2O2��ˮ��Ӧ���ɵ�����uΪ������tΪNaOH�������Ͱ�����Ӧ���ɵ�rΪ������sΪ�Ȼ�泥��Ȼ�狀��������ƻ�ϼ������ɰ�����ˮ���Ȼ��ƣ�����vΪNaCl��A��ʵ������ȡNH3���Ȼ�狀���ʯ�һ�ϼ��ȣ���O2������غͶ������̻�ϼ������������ô��Թܼ���װ�ý��У���A��ȷ��B���ɷ�����֪����������Ԫ��V��W��X��Y��Z����ΪH��N��O��Na��Cl�������Ƶ�ԭ�Ӱ뾶�ڶ���������Ԫ�������N��O�˵������ԭ�Ӱ뾶С����ԭ�Ӱ뾶Na>N>O����B����C����Ӧ�����û���Ӧ������Ӧ��Na2O2��ˮ��Ӧ����������NaOH�ķ�Ӧ�����û���Ӧ����C����D��Cl2����NaOH����NaCl��NaClO��ˮ��Cl2������ԭ������������������D����ΪD��


 ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д� Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д� �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ�������ȷ�Ӧ���ǣ�������
A.ľ̿ȼ��
B.���ȷ�Ӧ
C.����ʯ��ʯ
D.�������ƺ����ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ѣ�CH3OCH3������Ϊ21���͵�����ȼ�ϣ�����ࡢ��Ч�����������Ļ������ܣ�������һ����ɫ���壬������������ζ����ȼ����Ϊ1455kJ/mol�����ѿ���ȼ�ϵ�ص�ȼ�ϣ�
��1����֪H2��g����C��s����ȼ���ȷֱ���285.8kJmol��1��393.5kJmol��1�����㷴Ӧ4C��s��+6H2��g��+O2��g���T2CH3OCH3��g���ķ�Ӧ��Ϊ��
��2����ҵ������H2��CO2�ϳɶ����ѵķ�Ӧ���£�6H2��g��+2CO2��g��CH3OCH3��g��+3H2O��g����H��0
��һ���¶��£���һ���̶�������ܱ������н��и÷�Ӧ���������жϷ�Ӧ�ﵽ��ѧƽ��״̬������ѡ���ţ�ע���Сд��
a��c��H2����c��H2O���ı�ֵ���ֲ���
b����λʱ������2mol H2����ʱ��1mol H2O����
c�������������ܶȲ��ٸı�
d������������ѹǿ���ٸı�
���¶����ߣ��û�ѧƽ���ƶ����µ�ƽ�⣬CH3OCH3�IJ��ʽ�����������С�����䡱����ͬ������������ƽ��ʽ������
��3���Լ��ѡ�����������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�أ��õ�صĸ�����ӦʽΪ��
��4���ã�3���е�ȼ�ϵ��Ϊ��Դ����ʯīΪ�缫���500mL���з�̪��NaCl��Һ��װ����ͼ��ʾ����д����������Y�缫�����۲쵽����������ȼ�ϵ������2.8LO2����״���£�ʱ�������ʱ��NaCl��Һ��pH=��������Һ��������䣬����ȫ������Һ���ݳ�����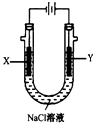
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ԫ�����ڱ��ش��������⣺
��1�����е�ʵ����Ԫ�����ڱ��IJ��ֱ߽磬����ͼ����ʵ�߲�ȫԪ�����ڱ��ı߽硣____________
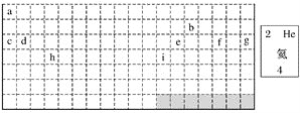
��2����������Ԫ�أ����ڶ�����Ԫ�ص���________����������Ԫ�ص���________��
��3��gԪ��λ�ڵ�________���ڵ�________�壻iԪ��λ�ڵ�________���ڵ�________�塣
��4��Ԫ��f�ǵ�________���ڵ�________��Ԫ�أ��밴��Ԫ�ص�ʽ��д����Ԫ�ص�ԭ��������Ԫ�ط��š�Ԫ�����ơ����ԭ��������____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����1.0 mL 0.1mol/L��ˮ�������ж���ȷ����
A. c��OH-��=c��NH4+�� B. ��1.0mL 0.1mol/L�����Ϻ���Һ������
C. ��Һ��pHС��13 D. ��������NH4Cl���壬c��OH-������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ڷ��ȷ�Ӧ���ǣ�������
A.����ʯ���м�ˮ
B.���������ˮ
C.Ũ�����ˮϡ��
D.��ʯ��ʯ����ʯ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��ʾ���л����У����������ŵ�ͬ���칹����Ŀ�����ǣ� ��
A.C4H10O
B.C4H10
C.C3H6O
D.C4H7Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��g��+B��g��![]() C��g��+D��g����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C��g��+D��g����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830��ʱ����һ��2L���ܱ������г���0.2mol��A��0.8mol��B����Ӧ��ʼ4s��A��ƽ����Ӧ����v��A��=0.005 mol/��L��s��������˵����ȷ����
A. 4sʱc��B��Ϊ0.78 mol/L
B. �÷�ӦAH>0
C. 830���ƽ��ʱ��A��ת����Ϊ20%
D. 1200��ʱ��ӦC��g��+D��g��![]() A��g��+B��g����ƽ�ⳣ��Ϊ2.5
A��g��+B��g����ƽ�ⳣ��Ϊ2.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ء���������������ɵĻ����Һ������c(H��)=0.2mol/L��c(Al3��)��0.2mol/L��c(SO42��)��0.5mol/L����c(K��)Ϊ�� ��
A. 0.1mol/L B. 0.2mol/L C. 0.3mol/L D. 0.4mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com