
分析 (1)根据化学式可知n(Al3+):n(SO42-)=2:3,据此计算SO42-的物质的量;
(2)先根据质量守恒定律来计算生成的C物质的质量,再利用M=$\frac{m}{n}$计算其摩尔质量;
(3)同种气体,其质量与分子数成正比,计算cg气体含有分子数目,然后根据n=$\frac{N}{{N}_{A}}$,V=n×Vm来计算.
(4)根据n=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$结合物质的构成计算,然后根据c=$\frac{n}{V}$计算所得溶液的浓度.
解答 解:(1)Al2(SO4)3中n(Al3+):n(SO42-)=2:3,故含0.4mol Al3+的Al2(SO4)3中所含SO42-的物质的量是0.4mol×$\frac{3}{2}$=0.6mol,
故答案为:0.6mol;
(2)16gA物质和20gB恰好完全反应生成0.04molC和31.76gD,由质量守恒定律可知,则C的质量为:16g+20g-31.76g=4.24g,C的摩尔质量为:$\frac{4.24g}{0.04mol}$=106g/mol,
故答案为:106g/mol;
(3)a克某气体中含有的分子数为b,则c克气体含有的分子数为$\frac{cb}{a}$,c克该气体的物质的量为:$\frac{\frac{bc}{a}}{{N}_{A}mo{l}^{-1}}$=$\frac{bc}{a{N}_{A}}$mol,在标准状况下Vm=22.4L/mol,则cg该气体的体积为:$\frac{bc}{a{N}_{A}}$mol×22.4L/mol=$\frac{22.4bc}{a{N}_{A}}$L,
故答案为:$\frac{22.4bc}{a{N}_{A}}$L;
(4)n(NH3)=$\frac{44.8L}{22.4L/mol}$=2mol,m(NH3)=2mol×17g/mol=34g;N(H)=3N(NH3)=2mol×3×NA/mol=6NA;n(N)=n(NH3)=2mol;
将2mol安全溶于水配成200mL的溶液,其物质的量浓度为:$\frac{2mol}{0.2L}$=10mol/L,
故答案为:34;6NA;2;10.
点评 本题考查物质的量的相关计算,为高频考点,侧重于学生的分析能力的考查,注意把握相关计算公式的运用,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 某溶液$\stackrel{+AgNO_{3}溶液}{→}$生成白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液$\stackrel{+NaOH溶液}{→}$生成蓝色沉淀,说明原溶液中有Cu2+ | |
| C. | 某溶液$\stackrel{+BaCl_{2}溶液}{→}$生成白色沉淀,说明原溶液中有SO42- | |
| D. | 某溶液$\stackrel{+KOH溶液}{→}$生成红褐色沉淀,说明原溶液中有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol/LNa2CO3溶液:c(Na+)=2c(H2CO3)+2 c(HCO3-)+c(CO32?) | |
| B. | 能使酚酞溶液呈红色的溶液:Na+、Ba2+、I-、NO3-可以大量共存 | |
| C. | 任何条件下,pH=1的硫酸溶液中:c(H+)=0.1mol/L | |
| D. | 将0.2 mol•L-1的HCN溶液和0.1 mol•L-1的NaOH溶液等体积混合,溶液显碱性,则c(HCN)=c(CN-)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2 的摩尔质量为95 g | |
| B. | 常温常压下,1 mol CO2的质量是44 g | |
| C. | 标准状况下,1 mol H2O所占的体积约为22.4 L | |
| D. | 100 mL 1mol/L的稀硫酸中含有H+ 的数目约为6.02×1022 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某化学小组设计如图装置,探究铜和一定量的浓HNO3是否反应是否有NO生成.已知:A试管内空气体积为50mL(标准状况),B广口瓶盛80mL水,硝酸不溶于煤油.
某化学小组设计如图装置,探究铜和一定量的浓HNO3是否反应是否有NO生成.已知:A试管内空气体积为50mL(标准状况),B广口瓶盛80mL水,硝酸不溶于煤油.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制造炊具 | B. | 制儿童玩具油漆 | C. | 制牙膏皮 | D. | 炼铝厂制造铝锭 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
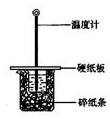 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 试剂 | 试管中的物质 |  | |
| A | 苯环对甲基的影响 | 酸性KMnO4溶液 | ①苯②甲苯 | |
| B | 比较Br-、Fe2+和I-的还原性 | 氯水 | ①FeBr2溶液②FeI2溶液 | |
| C | 苯分子中没有碳碳双键 | Br2的CCl4溶液 | ①苯②己烯 | |
| D | 探究接触面积对反应速率的影响 | VmL、cmol/L的盐酸 | ①ag大理石块②ag大理石粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
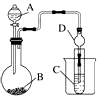 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com