
| A. | 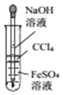 用所示装置制取并观察Fe(OH)2 | |
| B. | 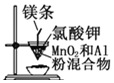 用所示装置制取金属锰 | |
| C. | 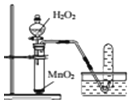 用所示装置制取干燥的O2 | |
| D. | 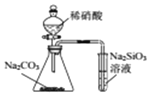 用所示装置比较N、C、Si的非金属性强弱 |
分析 A.四氯化碳的密度比水密度大,在下层;
B.点燃Mg条,引发铝热反应,冶炼高熔点的金属;
C.排水法收集氧气,不能得到干燥气体;
D.稀硝酸易挥发,硝酸与硅酸钠反应.
解答 解:A.四氯化碳的密度比水密度大,在下层,则不能防止生成的氢氧化亚铁被氧化,应选苯隔绝空气,故A错误;
B.点燃Mg条,引发铝热反应,冶炼高熔点的金属,则图中装置可制取金属锰,故B正确;
C.排水法收集氧气,不能得到干燥气体,应选排空气法,故C错误;
D.稀硝酸易挥发,硝酸与硅酸钠反应,则不能比较碳酸、硅酸的酸性及非金属性,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的制备和性质实验、非金属性比较为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:实验题
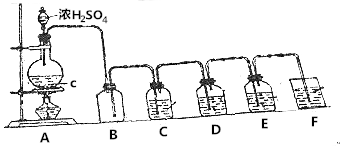 根据如图回答:
根据如图回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱溶液去油污:CO32-+H2O═HCO3-+OH- | |
| B. | 泡沫灭火器工作原理:2Al3++3CO32-+3H2O═2A1(OH)3↓+3CO2↑ | |
| C. | 明矾溶液中加入过量的氢氧化钡溶液:Al3++SO42-+Ba2++4OH-═BaSO4↓+AlO2-+2H2O | |
| D. | 用石墨为电极,电解Pb(NO3)2和Cu(NO3)2的混合溶液制取PbO2时,阳极上发生的电极反应式:Pb2++2 H2O-2e-═PbO2+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
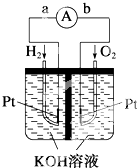 氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法.
氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X<W<Z<Y | |
| B. | 简单氢化物的稳定性:X>W>Z | |
| C. | 氢元素与W、X形成的相对分子质量最小的酸分子式为H2WX3 | |
| D. | X与Y形成的两种二元化合物中,阴、阳离子数之比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔的结构式为CH≡CH | B. | 甲烷分子的比例模型为 | ||
| C. | 碳原子的结构示意图为  | D. | 碳原子最外层电子的轨道表示式为 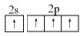 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
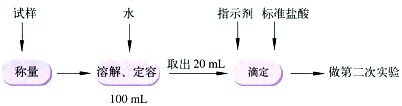
| 物质 | 样品 | 消耗的稀盐酸 | 反应后的溶液 |
| 质量(g) | 4.5g | 37.7g | 40g |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com