
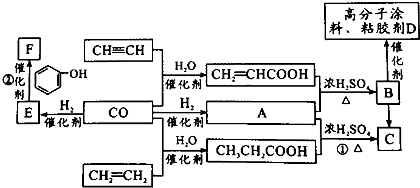
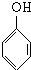
 +nHCHO$\stackrel{����}{��}$
+nHCHO$\stackrel{����}{��}$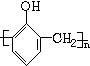 +nH2O��
+nH2O������ E��CO��H2�����ʵ���֮��Ϊ1��1��ȫ��Ӧ���ɣ������ʽΪCH2O���ҳ���������������걾�����뱽�ӷ�����Ӧ��EΪHCHO��FΪ��ȩ��֬��A��CO��H2�����ʵ���֮��Ϊ1��2��ȫ��Ӧ���ɣ����ʽΪCH4O����A�ܹ��������Ũ���������·���������Ӧ����AӦΪCH3OH���ٽ�ϻ���ϵ��֪BΪ��CH2=CHCOOCH3��CΪ��CH3CH2COOCH3��DΪ��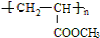 ���ݴ˽��н��
���ݴ˽��н��
��� �⣺E��CO��H2�����ʵ���֮��Ϊ1��1��ȫ��Ӧ���ɣ������ʽΪCH2O���ҳ���������������걾�����뱽�ӷ�����Ӧ��EΪHCHO��FΪ��ȩ��֬��A��CO��H2�����ʵ���֮��Ϊ1��2��ȫ��Ӧ���ɣ����ʽΪCH4O����A�ܹ��������Ũ���������·���������Ӧ����AӦΪCH3OH���ٽ�ϻ���ϵ��֪BΪ��CH2=CHCOOCH3��CΪ��CH3CH2COOCH3��DΪ��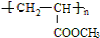 ��
��
��1����Ӧ�ٵĻ�ѧ����ʽΪ��CH3CH2COOH+CH3OH$��_{��}^{Ũ����}$CH3CH2COOCH3+H2O��Ϊ������Ӧ��Ҳ����ȡ����Ӧ��
BΪCH2=CHCOOCH3�����й�����Ϊ��̼̼˫����������
�ʴ�Ϊ��������Ӧ��ȡ����Ӧ����̼̼˫����������
��2��A��EΪHCHO����ά�صĻ�ѧʽ�ǣ�C6H10O5��n�����ߵ����ʽ��ͬ����A����
B��CH2=CH2����ʯ���ѽ�õ����ѻ���Ҫ�õ����ͣ���B����
C��CH2=CHCOOCH3����̼̼˫�����ɷ����Ӿ۷�Ӧ����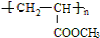 ����C��ȷ��
����C��ȷ��
D��BΪCH2=CHCOOCH3��CΪCH3CH2COOCH3��CH2=CHCOOH�к���̼̼˫����������ˮ�����ӳɷ�Ӧ��������ˮ���𣬹�D��ȷ��
�ʴ�Ϊ��AB��
��3����Ӧ��Ϊ��ȩ�뱽�ӷ�Ӧ�������ṩ�ǻ���λ�ϵ�������ԭ�ӣ�ȩ�ṩ�ʻ�����ԭ������ˮ��ȥ���Ӷ��������ɷ�ȩ��֬����Ӧ����ʽΪ��n +nHCHO$\stackrel{����}{��}$
+nHCHO$\stackrel{����}{��}$ +nH2O��
+nH2O��
�ʴ�Ϊ��n +nHCHO$\stackrel{����}{��}$
+nHCHO$\stackrel{����}{��}$ +nH2O��
+nH2O��
��4��CΪCH3CH2COOCH3��C��ͬ���칹���У�����NaOH��Һ��Ӧ���Ҳ����ܷ���������Ӧ��˵�����л����к���������ȩ����Ӧ��Ϊ�����������ṹ��ʽΪ��HCOOCH2CH2CH3��HCOOCH��CH3��2��
�ʴ�Ϊ��HCOOCH2CH2CH3��HCOOCH��CH3��2��
���� ���⿼���л��ƶϣ�Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ�������ѧ���ķ��������Ŀ��飬ע������л���Ľṹ���з����жϣ��Ƕ�ѧ���ۺ������������������Ŀ��飬����ʱע��������ʵ����ʣ�


 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HNO3��FeSO4��Fe2��SO4��3��Fe��NO3��3��N2O | B�� | Fe2��SO4��3��N2O��FeSO4��HNO3��Fe��NO3��3 | ||
| C�� | HNO3��Fe2��SO4��3��FeSO4��Fe��NO3��3��N2O | D�� | FeSO4��Fe��NO3��3��Fe2��SO4��3��HNO3��N2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10��ʱ��0.1mol/L Na2S2O3��0.1mol/L H2SO4��5mL | |
| B�� | 20��ʱ��0.1mol/L Na2S2O3��0.1mol/L H2SO4��5mL | |
| C�� | 10��ʱ��0.1mol/L Na2S2O3��0.1mol/L H2SO4��5mL����ˮ10mL | |
| D�� | 20��ʱ��0.2mol/L Na2S2O3��0.1mol/L H2SO4��5mL����ˮ10mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
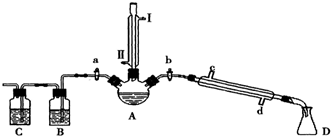
| ���� | �۵�/�� | �е�/�� |
| 1-���� | -89.5 | 117.3 |
| 1-�嶡�� | -112.4 | 101.6 |
| ���� | -95.3 | 142.4 |
| 1-��ϩ | -185.3 | -6.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����£�1.12LHCHO���еĵ�����Ϊ1.5NA | |
| B�� | 1mol����ϩ�к��е�̼̼˫����Ϊ4NA | |
| C�� | �����£�14g��ϩ�ͱ�ϩ�Ļ��������ԭ����Ϊ3NA | |
| D�� | 1.0L 0.1 mol•L-1��FeCl3��Һ�к���Fe3+��ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol•L-1��Na2CO3��Һ����������������Ϊ2NA | |
| B�� | ��״���£�22.4L NO������O2��ַ�Ӧ�����ɵ�NO2������ΪNA | |
| C�� | �����£�1mol SiC�к���Si-C������ĿΪ4NA | |
| D�� | ���³�ѹ�£�33.6L ����������������ַ�Ӧ��ת�Ƶ�����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
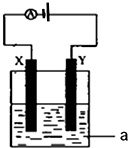 ��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���C��
��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���C���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com