
【题目】以废旧磷酸亚铁锂正极材料(主要成分为LiFePO4,含炭黑、铝等杂质)为原料可制备LiOH溶液和FePO4。
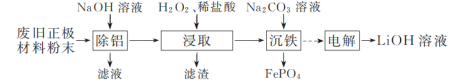
(1)“除铝”时反应的离子方程式为______________________________。
(2)试从沉淀溶解平衡移动的角度解释“浸取时加入H2O2、稀盐酸”可促进LiFePO4溶解的原因:______。
(3)“浸取”所得滤液中,磷元素的存在形式主要是________(填字母)。
a. PO![]() b. H3PO4 c. H2PO
b. H3PO4 c. H2PO![]()
(4)“沉铁”时铁、磷的沉淀率随溶液pH的变化如图1所示。pH>2.5后磷元素的沉淀率逐渐下降,原因是_____________________。
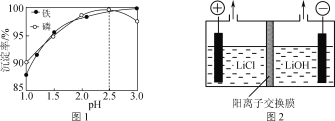
(5)“电解”制备LiOH的原理如图2所示,装置中使用阳离子交换膜将电解槽隔成阳极室和阴极室的目的是________________________________________。
(6)LiOH和(NH4)2Fe(SO4)2、H3PO4反应得到LiFePO4、NH4HSO4。写出该反应的化学方程式:__________________。
【答案】2Al+2H2O+2OH-=2AlO![]() +3H2↑ H2O2将Fe2+氧化,H+与PO
+3H2↑ H2O2将Fe2+氧化,H+与PO![]() 结合,溶液中c(Fe2+)和c(PO
结合,溶液中c(Fe2+)和c(PO![]() )减小,促进LiFePO4溶解平衡正向移动 c pH>2.5后,部分铁元素以Fe(OH)3形式存在,降低了磷元素的沉淀率 防止得到的LiOH不纯,且确保了工业生产的安全(以防H2、Cl2混合爆炸) (NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4↓+2NH4HSO4+H2O
)减小,促进LiFePO4溶解平衡正向移动 c pH>2.5后,部分铁元素以Fe(OH)3形式存在,降低了磷元素的沉淀率 防止得到的LiOH不纯,且确保了工业生产的安全(以防H2、Cl2混合爆炸) (NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4↓+2NH4HSO4+H2O
【解析】
废旧磷酸亚铁锂正极材料(主要成分为LiFePO4,含炭黑、铝等杂质)先与NaOH溶液反应,铝转化为偏铝酸钠进入溶液,过滤后用H2O2、稀盐酸浸取滤渣,LiFePO4反应溶解,亚铁离子被氧化,PO![]() 和氢离子反应生成H2PO
和氢离子反应生成H2PO![]() ,所以溶液主要有Li+、Fe3+、H2PO
,所以溶液主要有Li+、Fe3+、H2PO![]() 、Cl-等,滤渣为碳;加入碳酸钠溶液与H2PO
、Cl-等,滤渣为碳;加入碳酸钠溶液与H2PO![]() 反应生成二氧化碳和PO
反应生成二氧化碳和PO![]() ,继而得到FePO4沉淀;过滤后经系列处理得到LiCl溶液,电解得到LiOH溶液。
,继而得到FePO4沉淀;过滤后经系列处理得到LiCl溶液,电解得到LiOH溶液。
(1)除铝反应为铝单质和NaOH反应生成偏铝酸钠的反应,离子方程式为2Al+2H2O+2OH-=2AlO![]() +3H2↑;
+3H2↑;
(2)H2O2将Fe2+氧化,H+与PO![]() 结合,溶液中c(Fe2+)和c(PO
结合,溶液中c(Fe2+)和c(PO![]() )减小,促进LiFePO4溶解平衡正向移动;
)减小,促进LiFePO4溶解平衡正向移动;
(3)浸取时加入稀盐酸,H+与PO![]() 结合,磷酸为三元中强酸,所以此时磷元素的主要存在形式为H2PO
结合,磷酸为三元中强酸,所以此时磷元素的主要存在形式为H2PO![]() ,所以选c;
,所以选c;
(4)pH>2.5时溶液中氢氧根浓度较大,部分铁元素以Fe(OH)3形式存在,降低了磷元素的沉淀率;
(5)电解过程中阳极氯离子放电会产生氯气,氯气可以LiOH溶液反应,且与阴极产生的氢气混合容易爆炸,阳离子交换膜将电解槽隔成阳极室和阴极室可以防止得到的LiOH不纯,且确保了工业生产的安全(以防H2、Cl2混合爆炸);
(6)已知部分反应物和生成物,根据元素守恒可得方程式为(NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4↓+2NH4HSO4+H2O。


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
【题目】2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
A. 0.4mol
B. 0.2mol
C. 小于0.2mol
D. 大于0.2mol,小于0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和溴的取代反应的实验装置如图所示。其中A为带支管的试管改成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入铁屑粉少量。

(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式:____________、____________;试管C中苯的作用____________。
(2)反应开始后,D、E试管的现象分别为__________________、____________; E中所发生反应的离子方程式为____________。
(3)在上述整套装置中,具有防倒吸作用的仪器有(填字母) ____________。
(4)上述实验装置除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生命活动密切相关。以下是人体中血红蛋白、肌红蛋白与O2结合机制的相关研究,假定其环境温度均为36.8℃。
(1)血红蛋白Hb结合O2形成动脉血,存在反应①:HbH+(aq)+O2(g)![]() HbO2(aq)+H+(aq)。该反应可自发进行,则其ΔH______0(填“>”或“<”);血液中还同时存在反应②:CO2+H2O
HbO2(aq)+H+(aq)。该反应可自发进行,则其ΔH______0(填“>”或“<”);血液中还同时存在反应②:CO2+H2O![]() H++HCO3-,结合反应①②,肺部氧分压_____(填“较高”或“较低”)有利于CO2排出体外,从化学平衡角度解释原因 ____________。
H++HCO3-,结合反应①②,肺部氧分压_____(填“较高”或“较低”)有利于CO2排出体外,从化学平衡角度解释原因 ____________。
(2)肌肉中大量肌红蛋白 Mb也可结合O2形成MbO2,即反应③:Mb(aq)+O2(g)![]() MbO2(aq),其平衡常数K=
MbO2(aq),其平衡常数K=![]() 。其它条件不变,随着氧分压p(O2)增大,K值___(填“变大”、“变小”或“不变”)。已知在氧分压p(O2)=2.00 kPa 的平衡体系中,
。其它条件不变,随着氧分压p(O2)增大,K值___(填“变大”、“变小”或“不变”)。已知在氧分压p(O2)=2.00 kPa 的平衡体系中,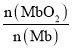 =4.0。吸入的空气中p(O2)=21 kPa,计算此时 Mb与氧气的最大结合度(平衡转化率)约为_______________(保留两位有效数字)。
=4.0。吸入的空气中p(O2)=21 kPa,计算此时 Mb与氧气的最大结合度(平衡转化率)约为_______________(保留两位有效数字)。
(3)Hb分子具有四个亚基,且每个亚基有两种构型(T型和R型)。图中,T0、R0表示未结合O2的T型和R型,且存在可逆的变构效应:T0![]() R0,正向平衡常数为K0;当四分子O2与Hb的四个亚基结合后,T4
R0,正向平衡常数为K0;当四分子O2与Hb的四个亚基结合后,T4![]() R4也是变构效应,正向平衡常数为K4。
R4也是变构效应,正向平衡常数为K4。
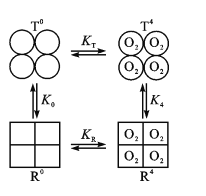
①已知某肺炎病人肺脏中T0+4O2![]() T4反应的n(O2)数据如下:
T4反应的n(O2)数据如下:
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
n(O2)/10-6 mol | 1.68 | 1.64 | 1.58 | 1.50 | 1.40 |
计算2.0 min~8.0 min内以T的物质的量变化表示的反应速率v(T4)为_________mol·min-1。
②现假定R型Hb对O2的结合常数为KR,T型Hb对O2的结合常数为KT。已知KR>KT,则图中K0____K4(填“>”或“<”)。
(4)氧气是生命活动必不可少的物质。如下图所示,以Pt为阳极,Pb(CO2)的载体,使CO2活化为阴极,电解经CO2饱和处理的KHCO3溶液可使氧气再生,同时得到甲醇。其阴极反应式为____;从电解后溶液中分离甲醇的操作方法是_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X与W同主族,Y原子的最外层电子数是其内层电子数的3倍,0.1 mol Z单质与足量盐酸反应产生H2的体积为3.36 L(折算成标准状况),W在元素周期表中的主族序数比其周期数大1。下列说法正确的是( )
A.XY2属于离子化合物
B.X的一种单质在高温下与WY2反应可制得W单质
C.原子半径:r(Z)>r(W)>r(Y)>r(X)
D.W的简单气态氢化物的热稳定性比Y的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚砷酸(H3AsO3)可用于白血病的治疗。室温下,配制一组c(H3AsO3)+c(H2AsO3-)+c(HAsO32-)+c(AsO33-)=0.100 mol·L-1的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是( )

A.pH=11的溶液中:c(HAsO32-)+c(AsO33-)>c(H2AsO3-)
B.c(Na+)=0.100 mol·L-1的溶液中:c(H2AsO3-)>c(H3AsO3)>c(HAsO32-)
C.c(Na+)=0.200 mol·L-1的溶液中:c(H+)+2c(H3AsO3)=c(OH-)+c(AsO33-)
D.pH=12.8的溶液中:c(H+)+c(Na+)>4c(H2AsO3-)+c(HAsO32-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与环境、科学、技术密切相关。下列有关说法中正确的是( )
A.华为首款5G手机搭载了智能的7nm制程SoC麒麟980芯片,此芯片主要成分是二氧化硅
B.用于制作N95型口罩的“熔喷布”主要原料是聚丙烯,聚丙烯的分子长链上无支链
C.国产飞机C919用到的氮化硅陶瓷是传统有机非金属材料
D.侯氏制碱法的工艺过程中应用了物质溶解度的差异
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B.![]() =1×10﹣15mol/L的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
=1×10﹣15mol/L的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C.与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D.水电离的c(H+)=1×10﹣15mol/L的溶液中:K+、Na+、AlO2﹣、CO32﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com