
分析 摩尔质量以g/mol作单位数值上等于其相对分子质量,相对分子质量为构成分子的各原子的相对原子质量之和,据此解答.
解答 解:①NaNO3化学式可知其相对分子质量=23+14+16×3=85,摩尔质量为85g/mol,
故答案为:85g/mol;
②SO3化学式可知其相对分子质量=32+16×3=80,其摩尔质量为80g/mol,
故答案为:80g/mol:
③电子质量忽略不计,NH4+离子符号可知相对式量=14+4×1=18,其摩尔质量为18g/mol,
故答案为:18g/mol;
④电子质量忽略不计,O22-离子符号可知,其相对式量=16×2=32,其摩尔质量为32g/mol,
故答案为:32g/mol.
点评 本题考查了摩尔质量的计算,明确摩尔质量与相对分子质量的关系是解本题关键,题目难度不大.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:多选题
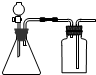
| A. | 将双氧水(H2O2)滴到MnO2中制取O2 | B. | 将浓盐酸滴到浓硫酸中制取HCl | ||
| C. | 将浓氨水滴到生石灰(CaO)中制取NH3 | D. | 将稀硫酸滴到锌粒上中制取H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4与足量稀 HNO3 反应:Fe3O4+8H+=2Fe3++Fe2++4H2O | |
| B. | 用小苏打治疗胃酸过多:NaHCO3+H+=Na++CO2↑+H2O | |
| C. | 双氧水中加入稀硫酸和 KI 溶液:H2O2+2H++2I-=I2+2H2O | |
| D. | 往碳酸氢钙溶液中滴入少量氢氧化钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是一种黄绿色、有刺激性气味、有毒的气体 | |
| B. | Cl2能使湿润的红色布条褪色 | |
| C. | Fe在Cl2中燃烧,生成的产物为FeCl2 | |
| D. | 实验室用加热二氧化锰和浓盐酸的方法制取Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
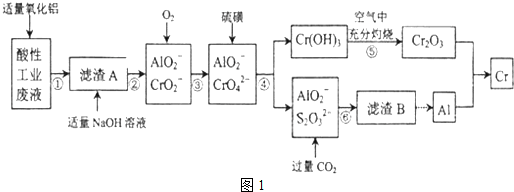
| 化合物 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| 完全沉淀的PH | 10.5 | 4.3 | 5.3 |
| 开始溶解的pH | -- | 7.8 | 9.2 |
| Ksp近似值 | 10-12 | 10-14 | 10-31 |
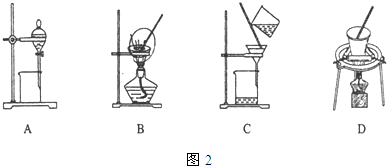
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1:1 | B. | 1:2 | C. | 3:1 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) | B. | c(HAc)>c(CH3COO-) | ||
| C. | 2c(H+)=c(CH3COO-)-c(CH3COOH) | D. | c(CH3COOH)+c(CH3COO-)=0.02mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com