
| 序号 | 组成 | 体积比 |
| 1 | ||
| 2 | ||
| 3 | ||
分析 根据CO2+2NaOH═Na2CO3+H2O、CO2+NaOH═NaHCO3来分析,溶质可能为NaOH和Na2CO3 ;Na2CO3;Na2CO3和NaHCO3 ;NaHCO3;所得溶液中含有两种物质的量相等的溶质,结合反应产物的几种可能确定溶质成分,根据氢氧化钠的物质的量确定参加反应的二氧化碳的物质的量,根据二氧化碳的量确定烯烃的可能情况,据此分析解答.
解答 解:①当CO2与NaOH的物质的量比小于1:2时,由反应CO2+2NaOH═Na2CO3+H2O溶质为碳酸钠,还有剩余的NaOH,
②当二氧化碳与NaOH的物质的量为1:2时,反应CO2+2NaOH═Na2CO3+H2O恰好完全进行,则溶液中的溶质为Na2CO3,
③当二氧化碳与NaOH的物质的量比大于1:2,而小于1:1时,发生CO2+2NaOH═Na2CO3+H2O、CO2+NaOH═NaHCO3,溶质为Na2CO3和NaHCO3 ;
④当二氧化碳与NaOH的物质的量比≥1:1时,发生CO2+NaOH═NaHCO3,溶质为NaHCO3;
溶质可能为NaOH和Na2CO3 ;Na2CO3;Na2CO3和NaHCO3 ;NaHCO3;300mL2mol/L的NaOH溶液n(NaOH)=CV=0.3L×2mol/L=0.6mol,0.1mol某种烯烃燃烧生成的二氧化碳完全被300mL2mol/L的NaOH溶液吸收,所得溶液中含有两种物质的量相等的溶质,可能为NaOH和Na2CO3 (各为0.2mol),Na2CO3和NaHCO3 (各为0.2mol),所需二氧化碳分别为0.2mol、
0.4mol.
(1)碳原子数均不超过5,若为纯净物,含有2个碳的烯烃为乙烯,分子式:C2H4,含有4个碳的烯烃为丁烯,分子式:C4H8,
故答案为:C2H4;C4H8;
(2)若为两种烯烃的混合物,碳、氢最简整数比为CH2,①C2H4、C5H10,体积比为x:y,$\frac{2x+5y}{4x+10y}$=$\frac{1}{2}$,解得x:y=1:2,②C3H6、C5H10,体积比为x:y,$\frac{3x+5y}{6x+10y}$=$\frac{1}{2}$,解得x:y=1:2,③C4H8、C4H8,体积比任意比,
故答案为:
| 序号 | 组成 | 体积比 |
| 1 | C2H4、C5H10 | 1:2 |
| 2 | C3H6、C5H10 | 1:1 |
| 3 | C4H8、C4H8 | 任意比 |
点评 本题考查有机物的推断及计算,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,注意把握烃的平均组成及原子守恒应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Cn(H2O)m | B. | (C2O3)n(H2O)m | C. | (C2H)n(H2O)m | D. | (CO)n(H2O)m |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| B. | 氢氧化铁溶胶、水玻璃、淀粉溶液均具有丁达尔效应 | |
| C. | 用二氧化碳生产聚碳酸酯可以减少碳排放,以减缓温室效应 | |
| D. | 双氧水、高锰酸钾溶液可以完全杀死埃博拉病毒,其消毒原理与漂白粉消毒的原理相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成纤维、光导纤维都属于有机高分子材料 | |
| B. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| C. | 天津港爆炸案对剧毒的氰化钠(NaCN)喷洒双氧水消毒,是利用了双氧水的氧化性 | |
| D. | 利用加热的方法杀死人体内感染的埃博拉病毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
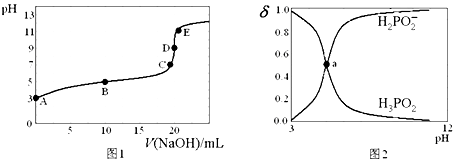
| A. | H3PO2的电离方程式为H3PO2?H2PO2-+H+ Ka≈10-5 | |
| B. | B点时,溶液中存在关系:2c(H+)+c(H2PO2-)═2c(OH-)+c(H3PO2) | |
| C. | C点时,溶液中存在关系:c(Na+)+c(H+)═c(H2PO2-)+c(OH-) | |
| D. | D点时,溶液中微粒浓度大小关系:c(Na+)>c(H2PO2-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
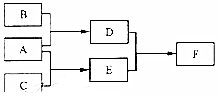 X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期,下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物,下列分析正确的是( )
X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期,下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物,下列分析正确的是( )| A. | 离子半径:Y>Z | B. | Z的含氧酸均为强酸 | ||
| C. | 与Y同周期氰化物中D最稳定 | D. | F含离子键和共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com