
 四种元素中只有一种是金属,下列说法错误的是( )
四种元素中只有一种是金属,下列说法错误的是( )| A. | 气态氢化物稳定性:R>Q | |
| B. | 元素T的离子结构示意图为 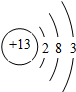 | |
| C. | 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键 | |
| D. | Q的一种同位素可用于测定文物的年代 |
分析 由元素在周期表中的位置可知,Q、R在元素周期表第二周期,T、W在元素周期表第三周期,由题意可知,T元素为金属,T为金属铝,Q为碳元素、R为氮元素、W为硫元素.
A.非金属性越强,对应气态氢化物越稳定;
B.元素T的离子即为铝离子的结构示意图;
C.同种原子形成共价键,两个原子吸引电子的能力相同,共用电子对不偏向任何一个原子,因此成键的原子都不显电性.这样的共价键叫做非极性共价键,相同原子形成的共价键为非极性键;
D.Q为碳元素,C-14具有放射性.
解答 解:由元素在周期表中的位置可知,Q、R在元素周期表第二周期,T、W在元素周期表第三周期,由题意可知,T元素为金属,T为金属铝,Q为碳元素、R为氮元素、W为硫元素.
A.非金属性越强,对应气态氢化物越稳定R的非金属性比Q的非金属性强,故气态氢化物稳定性:R>Q,故A正确;
B.铝原子变成铝离子失去最外层上的电子,所以铝离子的结构示意图为 ,故B错误;
,故B错误;
C.与S同主族的某元素形成的18电子的氢化物分子,即H2O2分子中既有H-O极性键又有O-O非极性键,故C正确;
D.Q是碳,C-14具有放射性,可用于测定文物的年代,故D正确.
故选B.
点评 本题考查原子结构和元素周期律,侧重考查学生分析判断能力,正确推断元素、明确元素周期律内涵、原子和物质结构是解本题关键,知道离子半径大小比较方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 元素性质 | 元素编号 | ||||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 原子半径(nm) | 0.073 | 0.075 | 0.152 | 0.110 | 0.099 | 0.186 | 0.143 |
| 最高正化合价 | 无 | +5 | +1 | +5 | +7 | +1 | +3 |
| 最低负化合价 | -2 | -3 | 无 | -3 | -1 | 无 | 无 |
| A. | ⑦的简单离子不是同周期元素离子半径最小的 | |
| B. | 气态氢化物的稳定性①>② | |
| C. | 气态氢化物的沸点高低②>④ | |
| D. | 阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不溶物只有铜 | |
| B. | 不溶物一定含铜,可能含铁 | |
| C. | 不溶物只有铁 | |
| D. | 溶液中一定含有Fe2+,可能含有Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ③能与水在一定条件下反应生成C
③能与水在一定条件下反应生成C
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
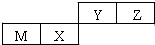
| A. | 原子半径Z>Y | |
| B. | Y的最高价氧化物对应水化物的酸性比X 的弱 | |
| C. | M和Y的最高价氧化物对应水化物之间能相互反应 | |
| D. | Y的气态氢化物比Z气态氢化物稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 54g H218O中含有电子总数为30NA个 | |
| B. | 11.2L H2中含有的电子数为NA个 | |
| C. | 23gNa+含有的最外层电子数为NA个 | |
| D. | 16g氧气和16g臭氧含有的核外电子总数均为8NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com