
【题目】NA代表阿伏加德罗常数。下列有关NA的叙述中,正确的是( )
A. 1 mol 任何物质所含的分子数均为NA
B. 14 g氮气所含的氮原子数为NA
C. 标准状况下,22.4 L水所含的水分子数为NA
D. 在钠与氯气的反应中,1 mol钠失去电子的数目为2NA
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】苯是一种重要的有机化工原料,广泛用于合成橡胶、塑料和医药等方面。下列关于苯的叙述正确的是( )
A. 分子式为C6H6B. 属于不饱和烃C. 能在空气中燃烧D. 无色无毒的液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次递增的前四周期元素,A元素的正化合价与负化合价的代数和为零;B元素原子的价电子结构为nsnnpn;C元素基态原子s能级的电子总数比p能级的电子总数多1;D元素原子的M能层全满,最外层只有一个电子。请回答:
(1)A元素的单质为A2,不能形成A3或A4,这体现了共价键的___性;B元素单质的一种空间网状结构的晶体熔点>3550℃,该单质的晶体类型属于________;基态D原子共有___种不同运动状态的电子。
(2)A与C形成的最简单分子的中心原子杂化方式是___________,该分子与D2+、H2O以2:1:2的配比结合形成的配离子是_________(填化学式),此配离子中的两种配体的不同之处为_____(填标号)。
①中心原子的价层电子对数 ②中心原子的孤电子对的对数 ③中心原子的化学键类型 ④VSEPR模型
(3)1molBC—中含有的π键数目为______;写出与BC-互为等电子体的分子和离子各一种______、______。
(4)D2+的硫酸盐晶体的熔点比D2+的硝酸盐晶体的熔点高,其原因是______。
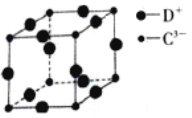
(5)D3C具有良好的电学和光学性能,其晶体的晶胞结构如图所示,D+和C3—半径分别为apm、bpm,D+和C3—都是紧密接触的刚性小球,则C3—的配位数为_____,晶体的密度为____g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产、生活中具有广泛的应用。下列生产、生活中的事例不涉及氧化还原反应的是
A. 金属冶炼 B. 燃放鞭炮
C. 食物腐败 D. 点制豆腐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物:①正丁烷,②丙烷,③2—甲基丁烷,④异丁烷,⑤己烷。沸点由高到低的顺序为( )
A. ②①④③⑤B. ⑤③④①②C. ⑤③①④②D. ②①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有碘水的试管中加入适量四氯化碳后振荡,静置片刻后现象为( )
A. 溶液呈紫色
B. 溶液呈棕色
C. 分层,下层为紫色
D. 分层,上层为紫色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com