
苯分子中的碳碳键不是单双键交替的,不能作出这种判断的证据是
A.苯的邻位二元取代物只有一种 B.苯环中碳碳键均相同
C.苯的一元取代物无同分异构体 D.苯不使酸性KMnO4溶液褪色
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:选择题
铅蓄电池的示意图如图所示。下列说法正确的是

A.放电时,N为负极,其电极反应式为: PbO2+SO42-+4H++2e-=PbSO4+2H2O
B.放电时,c(H2SO4)不变,两极的质量增加
C.充电时,阳极反应式为:PbSO4+2e-= Pb+SO42-
D.充电时,若N连电源正极,则该极生成PbO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列关于新制氯水及久置氯水的说法,不正确的是
A.新制的氯水呈黄绿色,久置的氯水无色
B.新制的氯水漂白作用强,而久置的氯水漂白作用很弱
C.新制的氯水所含成分的种类多,而久置的氯水所含成分的种类较少
D.新制的氯水中无氯离子,而久置的氯水中则含氯离子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中考试化学试卷(解析版) 题型:填空题
(9分)依据事实,写出下列反应的热化学方程式。
(1)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。 放出571.6kJ的热量,
表示H2燃烧的热化学方程式为_____ _____ ____。
(2)在25℃、101kPa下,1g甲醇液体燃烧生成CO2和液态水时放热22.68kJ。 则表示甲醇
燃烧热的热化学方程式为__________________________________________ ______
(3)已知:已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol一1
H2(g)+ O2(g)=H2O(g) ΔH=-285.8 kJ·mol一1
O2(g)=H2O(g) ΔH=-285.8 kJ·mol一1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol一1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol一1
则煤的气化主要反应(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式是
_______________________________________
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
化学反应可视为旧键短裂和新键形成的过程。共价键的键能是两种原子间形成1mol共价键(或其可逆过程)时释放(或吸收)的能量。已知H-H 键的键能为436kJ·mol-1 ,Cl-Cl键的键能为243 kJ·mol-1 ,H-Cl键的键能为431 kJ·mol-1 ,则H2 (g ) + Cl2 (g ) == 2HCl(g ) 的反应热(△H )等于
A.-183 kJ·mol-1 B.183 kJ·mol-1 C.-862 kJ·mol-1 D.862 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列操作中属于物理变化的是
A.重油在催化剂作用下进行裂化 B.石油高温时裂解成短链的烃
C.把煤隔绝空气加强热进行干馏 D.把煤焦油加热进行分馏
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:填空题
(8分)下图表示的是向Na2CO3溶液中滴入稀盐酸(单位为ml)时产生CO2的过程。
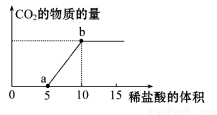
(1)写出a点以前发生反应的离子方程式:
(2)写出a到b点发生反应的离子方程式:
(3)若某Na2CO3溶液中含84.8g Na2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO3-的物质的量之比为2∶1,则滴入的稀盐酸中的HCl的物质的量为 mol(保留小数点后两位数字)。
(4)已知HCO3-+OH-=== CO32-+H2O ,若某溶液中含1 mol NaHCO3,滴入一定量的稀NaOH,恰好使溶液中Na+ 和HCO3-的物质的量之比为2:1,则滴入的NaOH的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:选择题
下列状态的物质,既能导电又属于电解质的是
A.K 2SO4晶体 B.NaCl溶液 C.液态HCl D.熔融的KOH
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:填空题
(16分)海水中含有非常丰富的化学资,从海水中可提取多种化工原料。下图是某工厂对海水资综合利用的示意图。
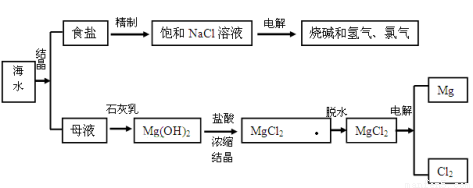
试回答下列问题:
(1)我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为 价。
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是 ①③(填序号)。
(3)写出电解饱和食盐水的化学方程式 ,当转移0.2mol电子时,阴阳两极生成的气体体积之和是 (标准状况下)。
(4)以海边贝壳为原料可以制取石灰乳,贝壳的主要化学成分为 (写化学式)。
(5)目前,世界上生产的镁有60%自海水,由“母液”制“镁”的过程中,发生了 个复分解反应(填数目)。
(6)电解氯化镁所得的氯气,除用于生产盐酸外,还可以用于制取漂白粉,漂白粉的有效成份
是 (写化学式)。
(7)溴主要以Br-形式存在于海水中,提取食盐后剩下的母液(也叫卤水)中,Br-的浓度较大,工业上 制备的Br2的操作步骤为:一定条件下,将Cl2通入卤水中,生成Br2,利用热空气将Br2吹出,Br2可用热空气吹出,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com