
下面关于化学反应的限度的叙述中,正确的是
A.化学反应的限度都相同
B.可以通过改变温度控制化学反应的限度
C.可以通过延长化学反应的时间改变化学反应的限度
D.当一个化学反应在一定条件下达到限度时,反应即停止
科目:高中化学 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:实验题
废弃物的综合利用既有利于节约资源,又有利于保护环境。工业上利用铅浮渣(主要成分是PbO、Pb还含有少量的Ag、CaO)可制备硫酸铅。制备流程图如下:

下表是25℃ 时某些盐的浓度积常数:
化学式 | CaSO4 | Ag2SO4 | PbSO4 |
Ksp | 4.9×10-5 | 1.2×10-5 | 1.6×10-8 |
(1)实验室用75%的硝酸来配制15%的硝酸溶液,不需用到的玻璃仪器有 (填标号)。
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒
(2)步骤I有NO产生,浸出液中含量最多的金属阳离子为 Pb2+,写出Pb参加反应的化学方程式 ,为防止Ag被溶解进入溶液,步骤I操作时应注意 。
(3)母液可循环利用于步骤I,其溶质主要是 (填一种物质化学式),若母液中残留的 SO42-过多,循环利用时可能出现的问题是 。
(4)粗PbSO4 产品含有的杂质是____________,需用 溶液多次洗涤,以得到纯净的PbSO4。
(5)铅蓄电池放电时正极的电极反应式为 。如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.80 L,电解前硫酸溶液浓度为4.50 mol·L-1,当制得4.48 LCl2时(在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)_________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:选择题
2015年10月,屠哟哟获得诺贝尔生理学或医学奖,理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率。她成为首获科学类诺贝尔奖的中国人。青蒿素两步可合成得到治疗疟疾的药物青蒿琥酯。下列有关说法正确的是
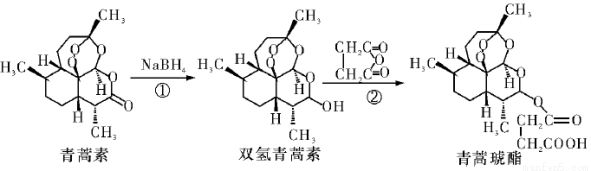
A.青蒿素分子式为C15H24O5
B.反应②原子利用率为100%
C.该过程中青蒿素生成双氢青蒿素属于氧化反应
D.1 mol青蒿琥酯与氢氧化钠溶液反应,最多消耗1 mol氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.放热反应不一定不需要加热,但吸热反应一定需要加热
B. 中和反应都是放热反应
C.氢气燃烧放出大量的热,说明参加反应的氢气和氧气总能量比生成物水的总能量低
D.C与CO2反应是吸热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
将固体NH4Br置于密闭容器中,在某一温度下,发生下列反应:NH4Br(g) NH3(g) + HBr(g)
NH3(g) + HBr(g)
2HBr(g) H2(g) + Br2(g) ,两分钟后测得c(H2)为0.5mol/L-1,c(HBr)为4mol/L-1,若NH4Br的分解速率用v(NH3)表示,下列速率正确的是
H2(g) + Br2(g) ,两分钟后测得c(H2)为0.5mol/L-1,c(HBr)为4mol/L-1,若NH4Br的分解速率用v(NH3)表示,下列速率正确的是
A.0.5mol·L-1·min-1 B .2.5 mol·L-1·min-1
C.2 mol·L-1·min-1 D.5 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
若短周期中的两种元素可以形成原子个数比为2:3的化合物,则这两种元素的原子序数之差不可能是
A.1 B.3 C.5 D.6
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:填空题
(1)工业合成氨的反应:N2+3H2= 2NH3是一个放热反应。已知该反应生成2mol NH3放出92kj热量。如果1 mol N2和3 mol H2混合,使其充分反应,放出的热量_____(“大于”、“小于”、“等于”)上述数值,其原因是___________。
(2)将4molA气体和2mol B气体在2L的密闭容器中混合并在一定条件下发生如下反应 2A(g)+ B(g) 2C(g)过2s测得C的浓度为0.6mol/L,则用物质A表示的平均反应速率为_____, 2s时物质A的转化率为_____,2s时物质B的浓度为_____。
2C(g)过2s测得C的浓度为0.6mol/L,则用物质A表示的平均反应速率为_____, 2s时物质A的转化率为_____,2s时物质B的浓度为_____。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:选择题
现有部分短周期元素的性质或原子结构如下表:
元素符号 | 元素性质或原子结构 |
T | M层上的电子数是原子核外电子层数的2倍 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
下列叙述中不正确的是
A.14X可用与测定文物年代 B.Z的非金属性比T强
C.Y和T位于同一主族 D.X元素形成的化合物种类很多
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市等十校高三3月联考理综化学试卷(解析版) 题型:填空题
Ⅰ、单质硅由于其成熟的生产工艺, 丰富的生产原料及优异的性能被广泛用于电子行业及太阳能电池的生产等,在二氧化碳氛围中通过利用金属钠来还原二氧化硅可在较低的温度条件下得到硅,同时生成一种盐X,这相比起现有的生产工艺具有节约能耗的优势。
(1)写出上述制备硅的化学反应方程式 。
(2)二氧化硅与二氧化碳物理性质差别很大,原因是 。
(3)盐X的溶液能与Al2(SO4)3溶液反应生成一种白色沉淀和气体。写出此反应的离子反应方程式 。
Ⅱ(12分)某盐A有3种元素组成,易溶于水。将A加热,生成既不助燃,也不使湿润的红色或蓝色石蕊试纸变色的气体B和H2O。将A溶于水,进行下列实验:①酸性条件下与H2S作用生成淡黄色沉淀C,同时放出无色气体D,D在空气中转变为红棕色气体E;②当通入足量Cl2时,无明显现象,但将所得溶液浓缩后即可得到无色晶体盐F。请回答下列问题:
(1)写出A的化学式: ; B的电子式: 。
(2)写出上述实验①、②所发生的离子反应方程式:
① ;② 。
(3)D、E对环境有危害,可用NaOH溶液来吸收等物质的量的D、E混合气体,写出其化学反应方程式 。
(4)判断盐F的可能成份 ;
设计实验方案确定F的成份 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com