
| A. | 正、逆反应速率都减小,平衡向逆反应方向移动 | |
| B. | 正、逆反应速率都增大,平衡向逆反应方向移动 | |
| C. | 逆反应速率增大,正反应速率减小,平衡向正反应方向移动 | |
| D. | 逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:选择题
 某有机物A的化学式为C6H12O2,已知A~E有如图所示的转化关系,C能发生银镜反应而E不能,则A的结构可能有( )
某有机物A的化学式为C6H12O2,已知A~E有如图所示的转化关系,C能发生银镜反应而E不能,则A的结构可能有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡可作胃酸的中和剂 | |
| B. | 还原铁粉用作食品抗氧化剂 | |
| C. | 铁红常用制作红色油漆和涂料 | |
| D. | FeCl3溶液能和Cu反应,可用于铜质印刷线路板制作 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,溶液的pH会增大 | |
| B. | 加入少量固体NaOH,溶液中c(CH3COO-)+c(OH-)>c(Na+)+c(H+) | |
| C. | 加入少量0.1mol•L-1的硫酸,水电离产生的c(H+)减小 | |
| D. | 与0.1mol•L-1的NaOH溶液等体积混合后,溶液中c(CH3COO-)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青铜、不锈钢都是合金 | |
| B. | 铜在空气中会生成铜诱 | |
| C. | 多数合金的熔点高于组成它的成分金属的熔点 | |
| D. | 铝是活泼金属,但在空气中耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
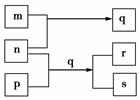 元素W、X、Y、Z的原子序数依次增加.p、q、r是由这些元素组成的二元化合物.m、n分别是元素Y、Z的单质,m是生产、生活中运用最广泛的金属单质,n通常为深红棕色液体,r是一种强酸,p是来自于煤的一种常见有机物,s是难溶于水、比水重的油状液体.上述物质的转化关系如图所示.下列说法正确的是( )
元素W、X、Y、Z的原子序数依次增加.p、q、r是由这些元素组成的二元化合物.m、n分别是元素Y、Z的单质,m是生产、生活中运用最广泛的金属单质,n通常为深红棕色液体,r是一种强酸,p是来自于煤的一种常见有机物,s是难溶于水、比水重的油状液体.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 四种元素中存在第三周期元素 | |
| B. | W的氧化物常温常压下为液态 | |
| C. | 常温下将m投入浓硫酸中不发生任何反应 | |
| D. | p的最简式是CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com