

���� ��1�����ݽӴ���������Ĺ�ҵ���̺��豸��Ӧ�����жϣ��������������ڸ��������շ�Ӧ��
��2���������ڽӴ���ǰ������������������ϴ�ӡ������ֹ�����ж���Ӱ���������Ч����
���������ڽӴ����б���������������ѧ����ʽΪ2SO2+O2 $?_{��}^{����}$ 2SO3���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ��������������������IJ��ʣ�
��3����ѧƽ������÷�Χ�ǿ��淴Ӧ���ڹ�ҵ�Ӵ���������2SO2+O2 $?_{��}^{����}$ 2SO3Ϊ���淴Ӧ����ѧƽ���ƶ��������У�Ũ�ȡ��¶ȡ�ѹǿ������V2O5����������߷�Ӧ���ʣ��¶ȿ�����450�����ң��Ǹ���ʹ�����Ļ�����ǿȷ����ѹǿ���ó�ѹ����˸��ݻ�ѧƽ���ƶ�ԭ����ȷ��������ֻ��Ũ�ȣ�
��4��ͨ���������ܺ��������SO3�����϶࣬������2SO2+O2 $?_{��}^{����}$ 2SO3ƽ���ƶ���Ӱ�죻
��5����Ʒ����a��������Ũ�ȿɴ�120%��130%�������̵��ŵ��Ƕ�η�Ӧ��������գ����ԭ�ϵ������ʣ�
��6�����ݷ�Ӧ��ת����ϵʽ���㣬��ϵʽΪ��FeS2��2SO2��2SO3��2H2SO4��
��� �⣺��1���豸�����������������ڸ��������շ�Ӧ�ڷ���¯�н��У�����ʽΪ4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$ 2FeO3+8SO2��
�ʴ�Ϊ������¯��4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$ 2FeO3+8SO2��
��2���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������գ����ж�������Ĵ������ڴ�������Ϳ����е������Ӵ���Ӧ���������к���������������ʹ�����ж����������ջ������γɵ�¯�����뾭������ϴ�ӡ�������������ڽӴ����б���������������ѧ����ʽΪ2SO2+O2 $?_{��}^{����}$ 2SO3���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ��������������������IJ��ʣ����Ӧѡ����¹��̣�
�ʴ�Ϊ����ֹ�����ж������£�
��3�����������У�SO3����ȡ��Ӧԭ��Ϊ��2SO2+O2 $?_{��}^{����}$ 2SO3���÷�ӦΪ���淴Ӧ�����ݻ�ѧƽ��ԭ��Ϊ�����SO2��ת���ʣ�ͨ����������O2Ũ�ȵķ������ﵽʹSO2�����ܶ��ת��ΪSO3��Ŀ�ģ�
a����ʯ�������¯֮ǰ�ȷ��飬Ŀ����Ϊ�����������������ĽӴ��棬�ӿ�4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$ 2Fe2O3+8SO2 ��Ӧ���ʣ������Ǵ�2SO2+O2 $?_{��}^{����}$ 2SO3 ��Ӧ�л�ѧƽ��Ƕȿ��ǣ���a����ȷ��
b��ʹ��V2O5����������2SO2+O2 $?_{��}^{����}$ 2SO3 ��Ӧ��ֻ�ܼӿ�÷�Ӧ�����ʣ�����ʹƽ���ƶ�����b����ȷ��
c���Ӵ����д�ת����ʹ�����˵��¶ȣ�Ŀ����ʹ����������ǿ��ʹ��Ӧ������죬��ʵ���������¶ȣ����ʹ2SO2+O2 $?_{��}^{����}$ 2SO3 ƽ�������ȷ����ƶ����������ƶ������������SO2��ת���ʣ����ԽӴ����в�ʹ�úܸߵ��¶ȣ���c��ȷ��
d���ӷ���¯�г���������ɷ�ΪSO2��O2��N2��������������Ӵ��ң�¯����Ҫ�й����Ŀ�����������O2Ũ�ȣ����ʹ2SO2+O2 $?_{��}^{����}$ 2SO3 ƽ�������ƶ������������SO2��ת���ʣ���d��ȷ��
e���Ӵ����У�2SO2+O2 $?_{��}^{����}$ 2SO3������ѹǿ��ʹƽ�������ƶ����������������С�ķ�����Сѹǿ��ʹƽ�������ƶ������������������ķ����ڳ�ѹ�£�������ƽ�������ƶ������������SO2��ת���ʣ����ڸû�ѧƽ�⣬ѹǿ������ʹƽ�������ƶ���Ч���������ԣ����Թ�ҵ��ֱ�Ӳ��ó�ѹ�������������ø�ѹ��������e����ȷ��
f������������98.3%��Ũ��������SO3����ҪĿ���Ƿ�ֹ�����������谭SO3�����գ��뻯ѧƽ���ƶ�ԭ���أ���f����ȷ��
�ʴ�Ϊ��cd��
��4��ͨ���������ܺ��������SO3�����϶࣬��2SO2+O2 $?_{��}^{����}$ 2SO3��֪��������ƽ�������ƶ���
�ʴ�Ϊ�����������SO3�����϶࣬������SO2�Ĵ�������Ӧ���У�
��5����Ʒ����a��������Ũ�ȿɴ�120%��130%�������̵��ŵ��Ƕ�η�Ӧ��������գ����ԭ�ϵ������ʣ�
�ʴ�Ϊ����η�Ӧ��������գ����ԭ�ϵ������ʣ�
��6��������98%��H2SO4����Ϊx��
FeS2 ������������������������2H2SO4
120 2��98
200t��75%����1-10%����96%��95% 98%x
�б���ʽ��$\frac{120}{200t��75%����1-10%����96%��95%}$=$\frac{2��98}{98%x}$��
��� x=205.2 t��
�ʴ�Ϊ��205.2t��
���� ���⿼���˻�ѧ��ҵ�������̵ķ�����ʵ������Լ�������жϺͼ��㣬�ۺ���ǿ�����չ�ҵ��ȡ�����ԭ���������ǽ���Ĺؼ����Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
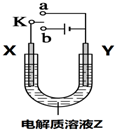
| A�� | ��X��Y��Z�ֱ�Ϊ��Ƭ��ͭƬ���Ȼ�ͭ��Һ������K��a���ӣ���Y���������ݷų� | |
| B�� | ��X��Y��Z�ֱ�Ϊ��Ƭ��ͭƬ���Ȼ�ͭ��Һ������K��a���ӣ�����Һ��Cu2+��Y���ƶ� | |
| C�� | ��X��Y��Z�ֱ�Ϊʯī��ʯī���Ȼ�ͭ��Һ������K��b���ӣ�����Һ��Cu2+��Y���ƶ� | |
| D�� | ��X��Y��Z�ֱ�Ϊʯī��ʯī���Ȼ�ͭ��Һ������K��b���ӣ��� Y�����л���ɫ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 44.80L | B�� | 58.24L | C�� | 80.64L | D�� | 116.48L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S+O2 $\frac{\underline{\;\;��\;\;}}{\;}$ SO2 | B�� | 4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$ 2Fe2O3+8SO2 | ||
| C�� | 2SO2+O2 $?_{����}^{����}$ 2SO3 | D�� | SO3+H2O=H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ˮ | |
| B�� | �ý��ݹ����������Һ�Ĺ���������ˮ�� | |
| C�� | ��װ�й轺����С������ | |
| D�� | �����������Ѵ���ҩ����ȡ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����
����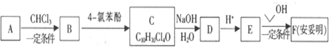
 ��
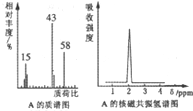
��
 ��
�� ��O2��Ӧ�Ļ�ѧ����ʽ2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��O2��Ӧ�Ļ�ѧ����ʽ2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��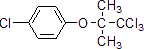 ��
��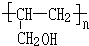 ��
��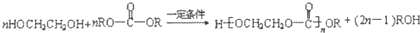
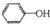 �������N��N��
�����м���N��N��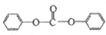 �ϳɹ�������M��
�ϳɹ�������M��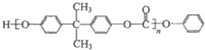 ��������N�ϳ�M�ľۺϷ�Ӧ����ʽΪn
��������N�ϳ�M�ľۺϷ�Ӧ����ʽΪn +n
+n $\stackrel{һ������}{��}$
$\stackrel{һ������}{��}$ +��2n-1��
+��2n-1�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 22.4L O2�ķ�����ԼΪNA | |
| B�� | ��״���£�11.2L H2O�ķ�����ԼΪ0.5NA | |
| C�� | 1 L 1mol/L��NaOH��Һ��Na+����ĿΪNA | |
| D�� | 0.1mol����������������ȫ��Ӧ����ʧȥ�ĵ�����Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������������Ƶ��ۻ� | B�� | ��ɱ������� | ||
| C�� | �Ȼ�����Ȼ��Ƶ��ܽ� | D�� | ����������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com