
| m2 |
| 197 |
| ||
| m1g |
| 12m2 |
| 197m1 |
| m2 |
| 197 |
| ||
| m1g |
| 12m2 |
| 197m1 |
| 12m2 |
| 197m1 |
| 12m2 |
| 197m1 |


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| 12w2 |
| 197w1 |
| 12w2 |
| 197w1 |
查看答案和解析>>
科目:高中化学 来源:2010年湖北省孝感高中高一下学期期末考试化学试题 题型:单选题
阅读下列一段话,回答10-11题。
2010年6月14日,美国宣布在阿富汗发现价值一万亿美元的未开采矿产资源,此矿藏富含Li,Fe, Cu, Au等元素。有分析家说:这可使阿富汗有望成为“锂业的沙特阿拉伯”,同时这也使阿富汗战争存在更大变数。
【小题1】锂经常被用来做锂电池,有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成的,电池总反应方程式为:8Li+3SOCl2 =6LiCl+Li2SO3+2S,已知亚硫酰氯和AlCl3?6H2O混合共热蒸干,可制得无水AlCl3。则下列叙述中正确的是( )
| A.电解质溶液中混入水,对电池反应无影响 |
| B.金属锂作电池的正极,石墨作电池的负极 |
| C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 |
| D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1 |
| A.工业上用铝单质与Fe2O3反应来大规模制备生铁 |
| B.可用焦碳与氧化铜高温反应制备铜 |
| C.古代“沙里淘金”是将金单质富积 |
| D.工业上由生铁炼钢以及由粗铜(含杂质较多的铜)制备纯铜都是进一步除去里面杂质 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮专题复习 常见非金属元素单质及其重要化合物练习卷(解析版) 题型:实验题
生铁中含碳和硫等元素。化学兴趣小组对某生铁样品进行了探究。根据要求回答下列问题。
Ⅰ.生铁中碳和硫元素的定性检验
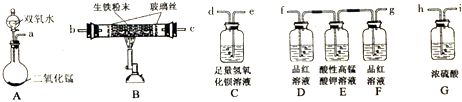
按如图装置进行实验(夹持仪器已略去,填接口字母代号)可以实现碳和硫元素的检验。

(1)仪器X的名称是 ;装置③⑤中试剂相同,装置④中盛放的试剂是 ?? 。
(2)写出甲中反应的化学方程式 。
(3)如果撤除装置③④⑤,能否确认生铁样品中碳元素的存在? ,理由是 。
Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量。称取样品w1 g进行实验,充分反应后,测得装置⑥中生成的沉淀为w2 g,该样品中碳的质量分数为 (用含w1、w2的式子表示)。
(5)乙同学认为,待一定量样品充分反应后,向装置④中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案测得的结果 (填“偏大”或“偏小”);若要提高硫元素含量的测定精度,在不改变实验原理的前提下,可以采取的一种措施是 。
查看答案和解析>>
科目:高中化学 来源:2010年湖北省高一下学期期末考试化学试题 题型:选择题
阅读下列一段话,回答10-11题。
2010年6月14日,美国宣布在阿富汗发现价值一万亿美元的未开采矿产资源,此矿藏富含Li,Fe, Cu, Au等元素。有分析家说:这可使阿富汗有望成为“锂业的沙特阿拉伯”,同时这也使阿富汗战争存在更大变数。
1.锂经常被用来做锂电池,有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成的,电池总反应方程式为:8Li+3SOCl2 =6LiCl+Li2SO3+2S,已知亚硫酰氯和AlCl3•6H2O混合共热蒸干,可制得无水AlCl3。则下列叙述中正确的是( )
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1
2.对于铁、铜、金的冶炼,下列说法错误的是( )
A.工业上用铝单质与Fe2O3反应来大规模制备生铁
B.可用焦碳与氧化铜高温反应制备铜
C.古代“沙里淘金”是将金单质富积
D.工业上由生铁炼钢以及由粗铜(含杂质较多的铜)制备纯铜都是进一步除去里面杂质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com