
| 反应温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 产品回收率(%) | 75.6 | 78.4 | 80.6 | 82.6 | 83.1 | 82.1 | 73.7 |
| 反应物料比 | 2:1 | 3:1 | 4:1 | 5:1 | 6:1 | 7:1 |
| 产品回收率(%) | 0 | 38.4 | 82. 6 | 83.6 | 84.5 | 84.8 |
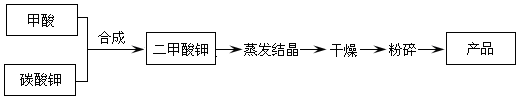
分析 (1)①由信息可知,甲酸与碳酸钾反应生成KH(HCOO)2,同时生成二氧化碳与水;
②根据表1中温度对产品回收率的影响判断,选择回收率高的温度,50~60℃该范围内回收率最高,温度再高回收率反而降低,由于甲酸易挥发性,可能是甲酸挥发导致;
根据表2中配比对回收率的影响判断,选择回收率高的配比,配比高于4:1时对产物回收率影响不变,会浪费原料;
(2)①滴定终点的pH值应在指示剂变色范围之内,二甲酸钾与氢氧化钠前后反应后溶液呈碱性,应选择酚酞为指示剂;滴定终点时溶液由无色变为浅红色且在半分钟内不褪色;
②令产品中二甲酸钾的质量分数为a,根据关系式KH(HCOO)2~NaOH列方程计算.
解答 解:(1)①由信息可知,甲酸与碳酸钾反应生成KH(HCOO)2,同时生成二氧化碳与水,反应方程式为:4HCOOH+K2CO3=2KH(HCOO)2+CO2↑+H2O,
故答案为:4HCOOH+K2CO3=2KH(HCOO)2+CO2↑+H2O;
②根据表1中温度对产品回收率的影响判断,选择回收率高的温度,50~60℃该范围内回收率最高,温度再高回收率反而降低,故选择50~60℃温度范围;
根据表2中配比对回收率的影响判断,选择回收率高的配比,配比高于4:1时对产物回收率影响不变,会浪费原料,故选择原料配比为4:1;
温度再高回收率反而降低,可能是由于温度过高,甲酸易挥发导致,
故答案为:50、60;4、1;温度过高,甲酸易挥发;
(2)①滴定终点的pH值应在指示剂变色范围之内,二甲酸钾与氢氧化钠前后反应后溶液呈碱性,应选择酚酞为指示剂;滴定终点时溶液由无色变为浅红色且在半分钟内不褪色,
故答案为:酚酞;溶液由无色变为浅红色且在半分钟内不褪色;
②令产品中二甲酸钾的质量分数为a,则:
KH(HCOO)2~NaOH
130g 1mol
2.5g×a×$\frac{25ml}{250ml}$ 0.0185L×0.1mol/L
所以130g:1mol=2.5g×a×$\frac{25ml}{250ml}$:0.0185L×0.1mol/L
解得a=96.2%,
故答案为:96.2%.
点评 本题考查有机物的合成、对数据的分析处理及实验条件的选择控制、中和滴定等,难度中等,是对学生综合能力的考查,计算质量分数是易错点,注意二甲酸钾为一元酸,确定二者为1:1反应是关键.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:选择题
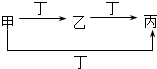 ( )
( )| 甲 | 乙 | 丙 | 丁 | |
| A | S | SO2 | SO3 | O2 |
| B | CO32- | HCO3- | CO2 | H+ |
| C | Cl2 | FeCl3 | FeCl2 | Fe |
| D | Al3+ | Al(OH)3 | AlO2- | NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
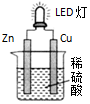
| A. | 锌是负极,电子从锌片经导线流向铜片 | |
| B. | 氢离子在铜片表面被还原 | |
| C. | 锌质量减少65g时,铜电极表面析出氢气是22.4L | |
| D. | 装置中存在“化学能→电能→光能”的转换 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
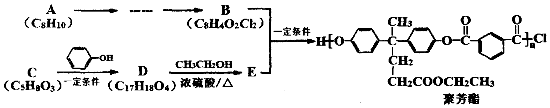
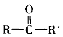 +2
+2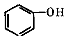 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$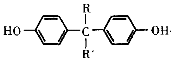 +H2O
+H2O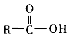 +SOCl2→
+SOCl2→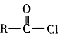 +SO2+HCl
+SO2+HCl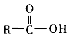 +R′OH→
+R′OH→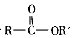 +HCl
+HCl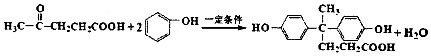 .
.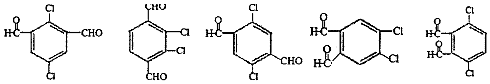 (其中两种).
(其中两种).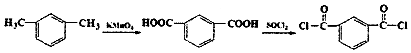 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、SO42-、Al3+、Cl- | B. | Na+、OH-、K+、Cl- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | K+、NO3-、I-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
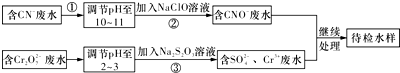
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
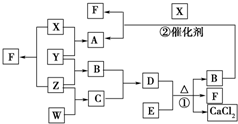 X、Y、Z、W均为气体单质,A、B、C均为无色气体化合物,D、E均为白色固体,F在通常情况下为无色无味的液体,它们有如下的转化关系:
X、Y、Z、W均为气体单质,A、B、C均为无色气体化合物,D、E均为白色固体,F在通常情况下为无色无味的液体,它们有如下的转化关系: ,F中的化学键类型为共价键.
,F中的化学键类型为共价键.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com