
| A. | 氢氧化铜与盐酸的反应 Cu(OH)2+2H+=Cu2++2 H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag | |
| D. | 碳酸钙溶于盐酸中 CaCO3+H+=Ca2++H2O+CO2↑ |
分析 A.反应生成氯化铜和水;
B.氢氧化钙完全电离;
C.电子、电荷不守恒;
D.反应生成氯化钙、水、二氧化碳,电荷不守恒.
解答 解:A.氢氧化铜与盐酸的反应的离子反应为Cu(OH)2+2H+=Cu2++2H2O,故A正确;
B.澄清的石灰水与稀盐酸反应的离子反应为OH-+H+=H2O,故B错误;
C.铜片插入硝酸银溶液中的离子反应为 Cu+2Ag+=Cu2++2Ag,故C错误;
D.碳酸钙溶于盐酸中的离子反应为CaCO3+2H+=Ca2++H2O+CO2↑,故D错误;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 化合物Z2O2含有离子键和极性共价键 | |
| B. | 原子半径大小:W>Z>X>Y | |
| C. | WO2能使品红溶液褪色,其漂白原理与氯水类似 | |
| D. | Y的气态氢化物与其最高价氧化物的水化物可反应生成盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫在空气中燃烧可以生成SO2,SO2在催化剂作用下可以被氧化为SO3,其热化学方程式可表示为:S(g)+O2(g)═SO2(g)△H=-297kJ/mol,SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-98.3kJ/mol.如图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6mol SO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量.
硫在空气中燃烧可以生成SO2,SO2在催化剂作用下可以被氧化为SO3,其热化学方程式可表示为:S(g)+O2(g)═SO2(g)△H=-297kJ/mol,SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-98.3kJ/mol.如图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6mol SO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Fe做还原剂 | B. | FeO做氧化剂 | ||
| C. | 铁元素的化合价降低 | D. | 铁元素化合剂升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 无机化合物可根据其组成和性质进行分类,
无机化合物可根据其组成和性质进行分类,| 物质类别 | 酸 | 碱 | 盐 | 酸性 氧化物 | 碱性 氧化物 |
| 化学式 | ①H2SO4、H2SO3、HNO3、H2CO3 ②H2S | ③NaOH、KOH、NH3.H2O ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2SO3、NaNO3、K2SO4、K2CO3、KNO3 | ⑦SO2 ⑧-- | ⑨-- ⑩-- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

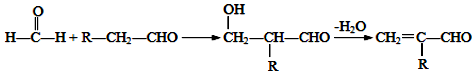
 .
.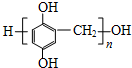 (写出一种即可).
(写出一种即可).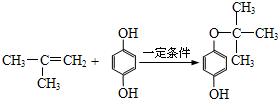 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com