
化工厂的设计是将实验室的研究成果转化为工业化生产的重要的基础工作。
(1)以硫铁矿为原料生产硫酸需经过 、 和 三个主要生产阶段。
(2)侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:
①索尔维制碱法的原理是 。(用化学方程式表示)
②侯氏制碱法与索尔维制碱法相比,优点是 。
③侯氏制碱法可以循环使用的物质有 。
(3)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12。海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 。
电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 。

 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
向一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2  5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
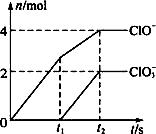
试回答:
(1)t2时,Ca(ClO)2与Ca(ClO3)2的物质的量之和为_________ mol,该石灰乳中含有的Ca(OH)2的质量是_________ g。
(2)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入氯气的速率不同,n(ClO-)和n (ClO3-)的比例也不同。若在原石灰乳中通入氯气的速率加快,则反应后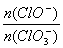 _____2(填“>”“<”或“=”)。
_____2(填“>”“<”或“=”)。
(3)若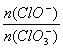 =a,则n(Cl-)=_________ mol(用含a的代数式表示)。
=a,则n(Cl-)=_________ mol(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列九种物质:①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:
| 分类标准 | 能导电 | 非电解质 | 电解质 |
| 属于该类的物质 |
|
|
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——物质结构与性质](1 5分)
四种短周期元素A、13、C、D的原子序数依次递增.其中A、B、C二种元素基态原子的2p能级上都有未成对电子.且术成对电子个数分别是2、3、2;D与C 可以形成D2C和D2C2两种化合物。回答下列问题:
(1)已知A元素与氢元素形成的某种气态化合物在标准状况下的密度为1.1 6 1 g·L-1,则在该化合物的分子中A原子的杂化方式为 。
(2)A、B、C二种元素的第一电离能由小到大的顺序为 (填元素符号)。
 (3)+1价气态基态阳离子再欠去一个电子形成+2价气态基态阳离子所需
(3)+1价气态基态阳离子再欠去一个电子形成+2价气态基态阳离子所需
要的能量称为第二电离能I2,依次还有I3、I4、I5……,推测D元素的电
离能第一次突增应出现在第电离能。
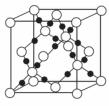
(4)AC2在高温高压下所形成的晶体其晶胞如图所示。该晶体的类型属于 晶
体.该品体中A原子轨道的杂化类型为 。
 (5)C和C形成原子个数比为1:3的常见离子.推测这两种微粒的空间
(5)C和C形成原子个数比为1:3的常见离子.推测这两种微粒的空间
构型为 。
(6)C和D形成的一种离子化合物D2C的品胞结构如图所示.该晶体中阳
离子的配位数为 。距一个阴离子周围最近的所有阳离子为顶点构成
的几何体为 。
已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA.则晶胞边长a= cm(用含ρ、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是
A.氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂
B.浓硫酸具有强氧化性,常温下可用铝罐盛装
C.氢氟酸具有弱酸性,可用氢氟酸雕刻玻璃
D.过氧化钠具有强氧化性,可用作潜水艇中氧气的来源
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列元素的半径为:
| 原子 | N | S | O | Si |
| 半径r/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
根据以上数据,磷原子的半径可能是( )
A.1.10×10-10m B.0.80×10-10m C.1.20×10-10m D.0.70×10-10m
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+3 ②ⅦA族元素是同周期中非金属性最强的元素 ③第二周期ⅣA族元素的原子核电荷数和中子数一定为6 ④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产、生活联系密切,下列说法正确的是
A.常用作净水剂的KAl(SO4)2和漂白粉都是强电解质
B.维生素C具有还原性,在人体内起抗氧化作用
C.对“地沟油”进行分馏可以获得汽油发动机的燃料
D.碘是人体必需的微量元素,所以要多吃富含高碘酸的食物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com