
分析 (1)根据物质的量、分子数、原子数之间的关系计算;
(2)根据同一化学式中各微粒的物质的量之比=微粒个数之比=系数之比计算;
(3)根据n=$\frac{m}{M}$计算5.3g Na2CO3 的物质的量,根据方程式计算溶液中n(HCl)、生成的二氧化碳的物质的量,根据c=$\frac{n}{V}$计算盐酸的物质的量浓度,根据V=nVm计算生成的二氧化碳的体积;
解答 解:(1)NO2 和N2O的物质的量相等,所以NO2 和N2O的分子数相等;一个NO2 分子中含2个O原子,一个N2O分子中含1个O原子,所以所含O原子个数之比为2:1;
其质量比等于其摩尔质量之比=46g/mol:44g/mo=l23:22;
故答案为:2:1; 23:22;
(2)Al2(SO4)3--2 Al3+--3SO42-
1 2 3
0.6 mol 1.2 mol 1.8 mol
所以Al2(SO4)3的物质的量为 0.6 mol,Al3+ 的物质的量为1.2 mol,
故答案为:1.2 mol;(1)2:1 23:22 (2)1.2
(3)5.3g Na2CO3 的物质的量为$\frac{5.3g}{106g/mol}$=0.05mol,则:
Na2CO3+2HCl=2NaCl+CO2↑+H2O
1 2 1
0.05mol n(HCl) n(CO2)
所以n(HCl)=0.05mol×2=0.1mol,n(CO2)=0.05mol,
故盐酸的物质的量浓度为$\frac{0.1mol}{0.02L}$=5mol/L,
生成二氧化碳的体积为:0.05mol×22.4L/mol=1.12L,
故答案为:5mol/l;1.12L.
点评 本题考查的是物质的量的有关计算,侧重考查学生对公式的掌握程度.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
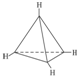 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2 | B. | KNO3 | C. | FeSO4 | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
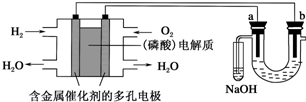
| A. | 电池工作时,正极反应式为O2+2H2O+4e-═4OH- | |
| B. | 电解时,a电极周围首先放电的是Cl-,而不是Br- | |
| C. | 电解时,电子流动路径是:负极-→外电路-→阴极-→溶液-→阳极-→正极 | |
| D. | 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.02 g H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
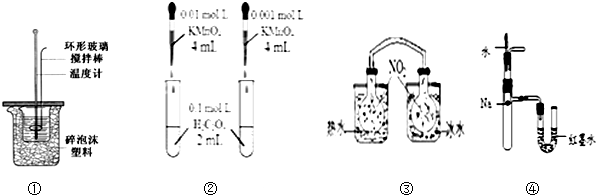
| A. | 装置①用于测定中和热装置 | |
| B. | 装置②依据褪色快慢比较浓度对反应速率的影响 | |
| C. | ③依据两容器内气体颜色变化,判断反应2NO2(g)?N2O4(g)平衡移动的方向 | |
| D. | 装置④依据U管两边液面的高低判断Na和水反应的热效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com