
下列有关化学实验的描述中正确的是
| A.分离乙醇和乙酸要用分液的方法 |
| B.配制一定物质的量浓度的NaCl溶液,如果NaCl固体中含有Na2CO3,所配制溶液中c(Na+)将偏高 |
| C.某无色溶液中加稀硫酸产生无色无味气体,该气体能使澄清石灰水变浑浊,说明该溶液中含CO32- |
D.平衡2NO2 N2O4(无色),减压时,气体颜色变浅,平衡向正反应方向移动 N2O4(无色),减压时,气体颜色变浅,平衡向正反应方向移动 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.用湿润的pH试纸测溶液的pH |
| B.用蒸馏法可将海水淡化为可饮用水 |
| C.常温下浓硫酸不能盛放在铝制容器中 |
| D.配制溶液时仰视容量瓶刻度线定容会使溶液浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验现象或结论错误的是
| 选项 | 实 验 | 现象或结论 |
| A | 取少量某溶液,滴加过量的稀盐酸无明显现象,再滴加BaCl2溶液 | 出现白色沉淀,则该溶液中含有SO42- |
| B | 相同温度下,取两份等质量的锌粒分别与足量稀酸反应,向其中一份中加入几滴CuSO4溶液 | 加入ZnSO4溶液的产生氢气快,最终二者生成氢气的量相同 |
| C | 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 | 反应速率:粉状大理石>块状大理石 |
| D | 向Na2S溶液中滴入ZnSO4溶液有白色沉淀生成,再加入几滴ZnSO4溶液 | 沉淀由白色转化为黑色,说明溶度积(Ksp):ZnS>CuS |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是 
①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤ 装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体
| A.①③⑤ | B.③⑤ | C.①②④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下面实验操作不能实现实验目的的是
| | 实验操作 | 目的 |
| A | 取绿豆大的钠分别加入到水和乙醇中 | 证明乙醇羟基中氢原子不如水分 子中氢原子活泼 |
| B | 取绿豆大的钠与钾分别投入水中 | 证明钾的金属性强于钠 |
| C | 将石蜡油在催化作用下,加强热产生的气 体通入溴的四氯化碳溶液中 | 证明产物不都是烷烃 |
| D | 蔗糖溶液加稀硫酸,水浴加热一段时间 后,加新制备的Cu(OH)2,加热 | 证明蔗糖水解后产生葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器(填编号) 。
(2)应称取Na2CO3的质量为
(3)有三瓶标签脱落的无色透明溶液,分别是稀盐酸、稀硫酸和稀硝酸。请你帮助实验老师设计两种方法鉴别它们,并贴上标签。
| | 操 作 步 骤 | 现 象 及 结 论 |
| 方法一 | | |
| 方法二 | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室模拟回收某废旧含镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等)生产Ni2O3。其工艺流程为: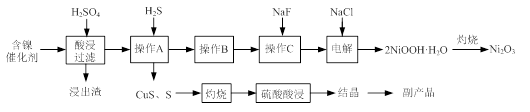
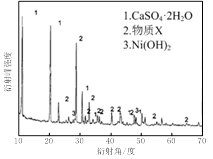
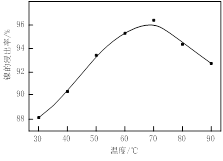
图Ⅰ 图Ⅱ
(1)根据图Ⅰ所示的X射线衍射图谱,可知浸出渣含有三种主要成分,其中“物质X”为 。图Ⅱ表示镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是 。
(2)工艺流程中“副产品”的化学式为 。
(3)已知有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com