
【题目】用Pb电极电解含有Cu2+和X3+均为0.1mol的溶液,阴极析出金属的质量m与溶液中通过电子的物质的量n关系如图,则离子的氧化性能力由大到小排列正确的是( )

A. Cu2+>X3+>H+ B. H+>X3+>Cu2+
C. X3+>H+>Cu2+ D. Cu2+>H+>X3+
科目:高中化学 来源: 题型:
【题目】微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用。请回答下列问題:
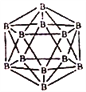
(1)区分晶体硼和无定形硼最可靠的科学方法为________。晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图)。若每个单元中有两个原子为10B,其余为11B,则该单元结构的类型有___种。
(2)NaBH4是一种重要的储氢载体,阴离子结构式为________。
(3)图1表示多硼酸根的一种无限长的链式结构,其化学式可表示为____(以n表示硼原子的个数)。
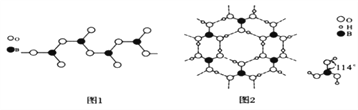
(4)硼酸晶体是片层结构,有与石墨相似的层状结构,图2表示的是其中一层的结构。硼酸晶体中存在的作用力有共价键、________、________。与H3BO3酸性最接近的是________(填字母)。
A.H4SiO4 B.H3PO4 C.HNO2
硼酸晶体在冷水中溶解度很小,但在热水中较大,原因是____________________。
(5)镁的堆积方式为________________,配位数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
I.氮氧化物的研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应: 2NO(g)+O2(g) ![]() 2NO2(g),下列状态能说明该反应达到化学平衡的是_______
2NO2(g),下列状态能说明该反应达到化学平衡的是_______
A.混合气体的密度保持不变 B.NO的转化率保持不变
C.NO和O2的物质的量之比保持不变 D.O2的消耗速率和NO2的消耗速率相等
(2)已知反应:2NO(g) ![]() N2(g)+O2(g) ΔH<0,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图象可以判断曲线R1、R2对应的是下列反应条件中的______ (填字母序号)。
N2(g)+O2(g) ΔH<0,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图象可以判断曲线R1、R2对应的是下列反应条件中的______ (填字母序号)。
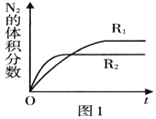
A.压强 B.温度 C.催化剂
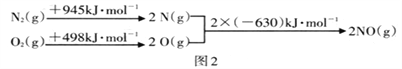
根据如图中的能量变化数据,计算反应:2NO(g) ![]() N2(g)+O2(g) 的ΔH=__________
N2(g)+O2(g) 的ΔH=__________
II.碳氧化物的研究
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) ΔH<0,现在体积为1L的恒容密闭容器(如图甲)中通入1molCO和2molH2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<0,现在体积为1L的恒容密闭容器(如图甲)中通入1molCO和2molH2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:

请回答:
T1_____ T2(填“>”或“<”或“=”)。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为_________ 。
(4)已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10-6 mol·L-1),需调节溶液pH范围为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) H=-632kJ·mol-1。下图为质子膜H2S燃料电池的示意图。下列说法错误的是( )

A. 电池工作时,电子从电极a经负载流向电极b
B. 实际工作中当反应生成64gS2时,电池内部释放632kJ电能
C. 电极a上发生的电极反应为:2H2S - 4e-=S2 + 4H+
D. 当电路中通过4mol电子时,有4molH+经质子膜进入正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述正确的是( )
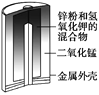
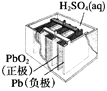
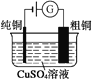
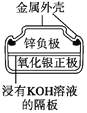
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
A. 图1所示电池中,MnO2的作用是催化剂
B. 图2所示电池放电过程中,硫酸浓度不断增大
C. 图3所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图4所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。 右图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。下列说法不正确的是( )

A. 腐蚀过程中,负极是c
B. 正极反应是 O2+ 4e-+2H2O = 4OH-
C. 若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为0.224L(标准状况)
D. 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羊通过吃草获得化合物和元素,那么羊和草体内的各种化学元素( )
A. 种类差异很大,含量大体相同 B. 种类和含量差异都很大
C. 种类大体相同,含量差异很大 D. 种类和含量都是大体相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,A与B可形成BA型化合物,且A元素是卤族元素中非金属性最强的元素;金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8;C元素有3种同位素C1、C2、C3,自然界中含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍;D的气态氢化物的水溶液呈碱性;而其最高价氧化物对应的水化物为强酸;E元素原子的最外层电子数比次外层电子数多4。
(1)写出下列元素的元素符号:A.________,B.______,C.________,D.________,E.________。
(2)写出C1、C2、C3三种原子的符号:C1________,C2________,C3________。
(3)E2-的结构示意图为________。
(4)A与B形成的化合物的化学式是_______,最常见的E原子与C2形成的分子中含________个中子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是( )。

A. 正极反应式:Ca+2Cl--2e-=CaCl2
B. 放电过程中,Li+向负极移动
C. 每转移0.1 mol电子,理论上生成20.7 g Pb
D. 常温时,在正、负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com