
| A、同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
B、 32gS8单质中含有的S-S键个数为NA(见图) |
| C、10L 0.1mol/L Na2S的水溶液中,S2-、HS-两种微粒数之和为NA个 |
| D、标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5NA |
| 32g |
| 32×8g/mol |


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠保存在石蜡油或煤油中 |
| B、用铁制或铝制容器运输浓硫酸、浓硝酸 |
| C、FeCl2溶液的试剂瓶中要放铁钉 |
| D、氢氧化钠溶液盛装在玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
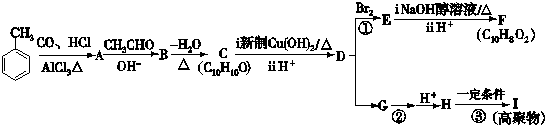
| CO、HCl |
| AlCl3△ |

| OH- |

| -H2O |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)+c(H+)>c(CO32-)+c(HCO3-)+c(OH-) |
| B、c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则一定a<b |
| D、若a=b,则溶液中c(HCO3-)>c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 分类标准 | 能导电 | 非电解质 | 电解质 |
| 属于该类的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
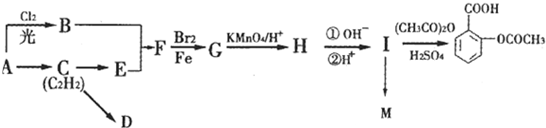
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的CH3COOH溶液的浓度小于pH=2的盐酸的浓度 |
| B、向NaHCO3溶液中加入少量NaOH固体,可抑制HCO3-的水解,使c(HCO3-)增大 |
| C、将任意量的CH3COOH溶液与NaOH溶液混合,其混合溶液均存在:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| D、Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)=c(HCO3-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com