
【题目】甲组同学拟用高锰酸钾制取氧气,并收集和测量氧气体积,其装置如图所示. 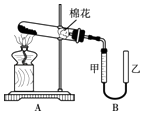
①读取装置B中收集到的气体体积时,需移动乙管与甲管中液面相齐,其目的是 .
②据报道高锰酸钾受热分解不产生MnO2 , 已知产气率= ![]() ×100%.若只发生KMnO4
×100%.若只发生KMnO4 ![]() KMnO2+O2↑,则产气率为 .
KMnO2+O2↑,则产气率为 .
③XRD谱显示还会分解产生K2MnO4和K2Mn4O8 , 写出分解产生这两种物质及氧气的化学方程式:
【答案】使得装置内外压强相等;20.25%;6KMnO4 ![]() 2K2MnO4+K2Mn4O8+4O2↑
2K2MnO4+K2Mn4O8+4O2↑
【解析】解:①读取装置B中收集到的气体体积时,需移动乙管与甲管中液面相齐,其目的是:使烧瓶中的压强与外界大气压相等,使读取的气体体积为外界大气压下的体积,
故答案为:使得装置内外压强相等;
②若只发生KMnO4 ![]() KMnO2+O2↑,则产气率=
KMnO2+O2↑,则产气率= ![]() ×100%=20.25%,
×100%=20.25%,
故答案为:20.25%;
③XRD谱显示还会分解产生K2MnO4和K2Mn4O8和氧气,结合电子守恒和原子守恒配平可知化学方程式为6KMnO4 ![]() 2K2MnO4+K2Mn4O8+4O2↑,
2K2MnO4+K2Mn4O8+4O2↑,
故答案为:6KMnO4 ![]() 2K2MnO4+K2Mn4O8+4O2↑.
2K2MnO4+K2Mn4O8+4O2↑.
①在反应前后应注意使左右两管液面相平,即使烧瓶中的压强与外界大气压相等,使读取的气体体积为外界大气压下的体积,在反应结束后,应先冷却气体的温度至室温,这样读取的气体的体积才是常温下的气体体积;
②配平书写化学方程式,结合产气率= ![]() ×100%,计算;
×100%,计算;
③XRD谱显示还会分解产生K2MnO4和K2Mn4O8和氧气,结合电子守恒和原子守恒配平书写化学方程式.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】化学与社会、生产、生活密切相关。下列说法正确的是
A.实验室从海带中提取单质碘的方法是取样→灼烧→溶解→过滤→萃取
B.从海水中提取物质都必须通过化学反应才能实现
C.为了增加食物的营养成分,可以大量使用食品添加剂
D.![]() 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物![]() ,该反应符合绿色化学的原则
,该反应符合绿色化学的原则
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质R完全燃烧的化学方程式为:2R+3O2 ![]() 2CO2+4H2O有关该反应,有下列说法:
2CO2+4H2O有关该反应,有下列说法:
①R一定含碳、氢两种元素,可能含有氧元素
②R中碳元素的质量分数是37.5%
③6.4g R完全燃烧,转移1.2NA个电子
④R的摩尔质量为32,若6.4g R完全燃烧生成8.8g CO2 ,
则正确的一组是( )
A.①②
B.③④
C.②④
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4mol·L-1HA溶液与0.2mol·L-1NaOH溶液等体积混合,测得混合溶液中c(Na+)﹥c(A-),则:
(1)混合溶液中c(A-)_________c(HA)(填“﹥”“﹤”或“=”)
(2)混合溶液中c(HA)+ c(A-)__________0.2mol·L-1(填“﹥”“﹤”或“=”)
(3)25℃时,如果取0.4 mol·L-1HA溶液与0.2mol·L-1NaOH溶液等体积混合,若测得混合溶液的pH=8,则c(Na+)-c(A-)=___________。(填准确数值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I向KI和硫酸混合溶液中加入过氧化氢溶液,迅速反应放出大量气泡,溶液呈棕色.
查阅资料知,反应过程如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO; ③H2O2+2HIO=I2+O2↑+2H2O
(1)用双线桥法表示过程①电子转移情况:H2O2+2KI+H2SO4=I2+K2SO4+2H2O
(2)上述实验过程②与③中,I2起到了的作用.
(3)试判断,酸性条件下HIO、H2O2、O2三种物质氧化性的强弱:(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于数以万计的化学物质和化学反应,分类法的作用几乎是无可替代的.
(1)现有下列5种物质:CuO、CO、MgO、Na2O、FeO.按照不同的分类标准,它们中有1种物质与其他4种物质有明显的不同,找出这种物质,并写出依据(写出两种):
①;
② .
(2)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,用简单的图示方法表示二者之间的关系 .
(3)生活中的食醋和豆浆分别属于分散系中的和 , 用可以鉴别(填化学专用名词).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3O4可表示为FeOFe2O3 , 是一种性能优良的新型磁性材料.水热法制备Fe3O4纳米级颗粒的反应为3Fe2++2S2O32﹣+O2+xOH﹣=Fe3O4+S4O62﹣+yH2O.下列说法中,不正确的是( )
A.每生成1mol Fe3O4 , 反应转移的电子总数为4mol
B.该反应中,氧化剂与还原剂物质的量之比为1:5
C.3mol Fe2+被氧化时,消耗O2标准状况下的体积约为22.4L
D.x=4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com