
| ����ʽ | �ṹ��ʽ | ��� | �۵� | �ܽ��� |
| C12H10ClN3O | 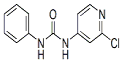 | ��ɫ�ᾧ��ĩ | 170��172��C | ������ˮ |
���� ��1��������Ԫ�ػ�̬ԭ�Ӻ������ȷ����ɶԵ�������������ˮ��Ϊ10��������
��2���۵�ϵ͵ľ���Ϊ���Ӿ��壻��ͬԪ��֮���γɼ��Լ���ͬ��Ԫ��֮���γɷǼ��Լ������ӹ��ɶԳƣ�������������ص��ķ���Ϊ�Ǽ��Է��ӣ�
��� �⣺��1�����ݹ���ԭ����֪����Ԫ�ػ�̬ԭ�Ӻ�����ӵ��Ų�ʽ��1s22s22p63s23p5�����ԳɶԵ�����Ϊ16����N��O��H֮���γɵ�10���ӷ���Ϊ������ˮ��������ˮ�����γ������
�ʴ�Ϊ��16��NH3��H2O��
��2������������۵�ϵͣ�������ˮ�������侧�������Ƿ��Ӿ��壻��ͬԪ��֮���γɼ��Լ���ͬ��Ԫ��֮���γɷǼ��Լ����÷����к��м��Լ��ͷǼ��Լ������ӹ��ɲ��Գƣ�����������IJ��ص������Է���Ϊ���Է��ӣ�
�ʴ�Ϊ�����ӣ����ԡ��Ǽ��ԣ����ԣ�
���� ���⿼���˹��ۼ��������Ų��������10����������Ŀ�ѶȲ������ڿ���ѧ���ķ���������Ӧ��������ע����ճ�����10�������Լ����Ӽ��Ե��жϷ�����


 �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д� ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
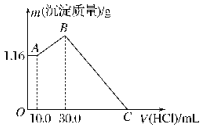 ��NaOH��MgCl2��AlCl3���ֹ�����ɵĻ������������ˮ����1.16g��ɫ����������������Һ����μ���1.00mol•L-1HCl��Һ������HCl��Һ����������ɳ����Ĺ�ϵ��ͼ��ʾ���Իش�
��NaOH��MgCl2��AlCl3���ֹ�����ɵĻ������������ˮ����1.16g��ɫ����������������Һ����μ���1.00mol•L-1HCl��Һ������HCl��Һ����������ɳ����Ĺ�ϵ��ͼ��ʾ���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ij��ѧ������ȤС��Ϊ̽��ͭ��Ũ���ᷴӦ�����������ʣ�������ͼ��ʾ��װ�õ���Ͻ���ʵ�飮
ij��ѧ������ȤС��Ϊ̽��ͭ��Ũ���ᷴӦ�����������ʣ�������ͼ��ʾ��װ�õ���Ͻ���ʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
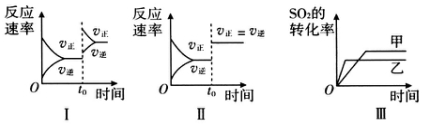
| A�� | ͼ���о�����t0ʱ������O2�����ʵ���Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� | |
| B�� | ͼ���о�����t0ʱ��ͨ�뺤��������ϵѹǿ�Է�Ӧ���ʵ�Ӱ�� | |
| C�� | ͼ���о�����t0ʱ�̼�������Ի�ѧƽ���Ӱ�� | |
| D�� | ͼ���о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϸ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 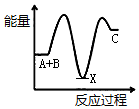 | B�� | 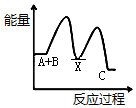 | C�� | 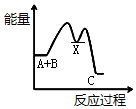 | D�� | 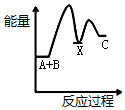 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=2��HA��Һ��pH=12��MOH��Һ����Ȼ�ϣ�c��H+��+c��M+���Tc��OH-��+c��A-�� | |
| B�� | 1 L 0.1 mol•L-1 ��NH4��2Fe��SO4��2����Һ�У�c��SO${\;}_{4}^{2-}$����c��NH${\;}_{4}^{+}$����c��Fe2+����c��H+����c��OH-�� | |
| C�� | 0.1 mol•L-1 NaHCO3��Һ�У�c��H+��+c��H2CO3���Tc��CO${\;}_{3}^{2-}$��+c��OH-�� | |
| D�� | 0.1mol•L-1��NaHA��Һ����pH=4��c��HA-����c��H+����c��H2A����c��A2-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com