
【题目】[化学——选修3:物质结构与性质]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]____________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________________,微粒之间存在的作用力是_____________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0, ![]() );C为(
);C为(![]() ,
, ![]() ,0)。则D原子的坐标参数为______。
,0)。则D原子的坐标参数为______。
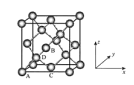
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a="565.76" pm,其密度为__________g·cm-3(列出计算式即可)。
【答案】(1)3d104s24p2;2;
(2)Ge原子半径大,原子间形成的σ单键较长,p-p轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键;
(3)GeCl4、GeBr4、GeI4的熔、沸点依次增高。原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强。
(4)O>Ge>Zn;
(5)sp3;共价键;
(6)①(![]() ,
, ![]() ,
, ![]() );②
);②![]() 。
。
【解析】试题分析:(1)Ge是32号元素,与碳元素是同一主族的元素,在元素周期表中位于第四周期IVA族;基态Ge原子的核外电子排布式为[Ar] 4s24p2,也可写为3d104s24p2;在其原子的最外层的2个4s电子是成对电子,位于4s轨道,2个4p电子分别位于2个不同的4p轨道上,所以基态Ge原子有2个未成对的电子;(2)Ge与C是同族元素,C原子原子半径较小,原子之间可以形成双键、三键;但Ge原子之间难以形成双键或三键,从原子结构角度分析,这是由于锗的原子半径大,原子之间形成的ρ单键较长,p-p轨道肩并肩重叠的程度很小或几乎不能重叠,难以形成π键;(3)锗元素的卤化物在固态时都为分子晶体,分子之间通过微弱的分子间作用力结合。对于组成和结构相似的物质来说,相对分子质量越大,分子间作用力越大,熔沸点越高。由于相对分子质量:GeCl4<GeBr4<GeI4,所以它们的熔沸点由低到高的顺序是:GeCl4<GeBr4<GeI4;(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。元素的非金属性越强,其吸引电子的能力就越强,元素的电负性就越大。元素Zn、Ge、O的非金属性强弱顺序是:O>Ge>Zn,所以这三种元素的电负性由大至小的顺序是O>Ge>Zn ;(5) Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为1个s轨道与3个p轨道进行的sp3杂化;由于是同一元素的原子通过共用电子对结合,所以微粒之间存在的作用力是非极性共价键(或写为共价键);(6) ①根据各个原子的相对位置可知,D在各个方向的1/4处,所以其坐标是(![]() ,
, ![]() ,
, ![]() );根据晶胞结构可知,在晶胞中含有的Ge原子数是8×1/8+6×1/2+4=8,所以晶胞的密度
);根据晶胞结构可知,在晶胞中含有的Ge原子数是8×1/8+6×1/2+4=8,所以晶胞的密度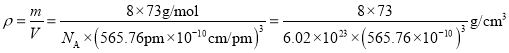 =
=![]() cm3。
cm3。


科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(NH2COONH4,简称甲铵)是CO2和NH3制尿素的中间产物,其中CO2反应生成甲铵的能量变化如下图所示。
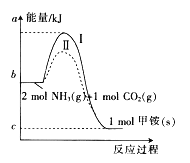
(1)图中反应为可逆反应,则生成甲铵的反应是 (填“放热”或“吸热”)反应。
(2)合成甲铵的热化学方程式为 。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,其原因是 。
(4)已知由甲铵合成尿素的反应为NH2COONH4(s)![]()
![]() ;
;![]() ,则由CO2(g)和NH3(g)直接合成固态尿素并生成液态水的热化学方程式为 。
,则由CO2(g)和NH3(g)直接合成固态尿素并生成液态水的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
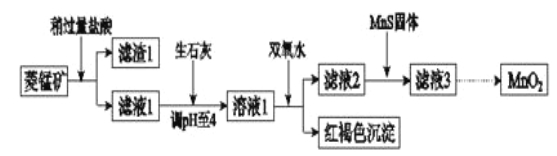
【题目】工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH) 2CO3等杂质]为原料制取二氧化锰,其流程示意图如下:
已知:生成氢氧化物沉淀的pH
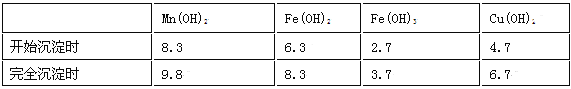
注:金属离子的起始浓度为0.1 mol/L,回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是 _______ ___________ 。盐酸溶解MnCO3的化学方程式是_______ ______________ ___ _____。
(2)向溶液1中加入双氧水时,反应的离子方程式是 _______ ___________ 。
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是 ________ 。
(4)将MnCl2转化为MnO2的一种方法是氧化法。其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:□Mn2++□ClO3-+□________=□________+□________+□________。
(5)将MnCl2转化为MnO2的另一种方法是电解法。
① 阳极生成MnO2的电极反应式是 ____ ___ ____________ _______ 。
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2。检验Cl2的操作是 _____ 。
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生。其原因是 ___ __ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的符号:
X___________;Y___________;Z___________;W___________;
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别
为_____________;___________________。
(3)由X、Y、Z所形成的离子化合物是_____________,(填化学式)它与W的最高价氧化物的水化物的浓溶液加热时的离子方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
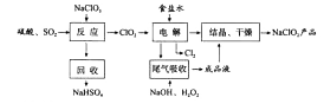
回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式_______。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据右图铜锌原电池示意图,回答下列问题:
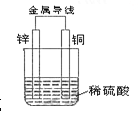
(1)该原电池总离子反应式是 。
(2)外电路电流的方向是从 (填Zn到Cu或Cu到Zn)。
(3)在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量 (填“增加”、“不变”或“减少”),电路中转移电子为 mol,铜表面析出了氢气 L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物。
(1)铁炭混合物在水溶液中可形成许多微电池。将含有Cr2O72–的酸性废水通过铁炭混合物,在微电池正极上Cr2O72–转化为Cr3+,其电极反应式为_____________。
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示。
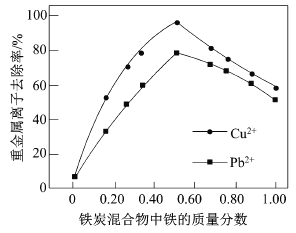
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是__________。
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_____________。
(3)纳米铁粉可用于处理地下水中的污染物。
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4–(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为 。
②纳米铁粉与水中NO3-反应的离子方程式为4Fe+NO3–+10H+===4Fe2++NH4++3H2O
研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是 。
③相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见图),产生该差异的可能原因是 。
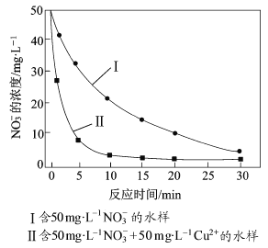
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A(C10H20O2)具有兰花香味,可用做香皂、洗发香波的芳香赋予剂。

已知:①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯原子取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 (选填序号)。
a、取代反应 b、消去反应 c、加聚反应 d、氧化反应
(2)C、D、F分子所含的官能团的名称依次是
(3)写出E的结构简式:
(4)写出C→D的化学方程式:
(5)写出B→F的化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下:

(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)===Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4 kJ·mol–1
Mg2SiO4(s)+4H+(aq)===2 Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4 kJ·mol–1
酸溶需加热的目的是______;所加H2SO4不宜过量太多的原因是_______。
(2)加入H2O2氧化时发生发应的离子方程式为___________。
(3)用下图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。
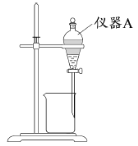
①实验装置图中仪器A的名称为_______。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,______、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水,______,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO3·3H2O。
[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全]。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com