
| A. | 称取8.0 g CuSO4,加入500 mL水 | |
| B. | 称取7.68 g CuSO4,加入480 mL水 | |
| C. | 称取12.5 g CuSO4•5H2O,加水配成500 mL溶液 | |
| D. | 称取12.0 g CuSO4•5H2O,加水配成480 mL溶液 |
分析 需要n(CuSO4)=n(CuSO4•5H2O)=0.10mol/L×0.5L=0.05mol,则m(CuSO4)=0.05mol×160g/mol=8.0g,m(CuSO4•5H2O)=0.05mol×250g/mol=12.5g,容量瓶配制溶液体积与容量瓶规格数值相同.
解答 解:需要n(CuSO4)=n(CuSO4•5H2O)=0.10mol/L×0.5L=0.05mol,如果称量的是硫酸铜,则m(CuSO4)=0.05mol×160g/mol=8.0g,如果称量的是胆矾,则m(CuSO4•5H2O)=0.05mol×250g/mol=12.5g,容量瓶配制溶液体积与容量瓶规格数值相同,所以需要配制500mL溶液,
故选C.
点评 本题以溶液配制为载体考查物质的量有关计算,为高频考点,明确配制溶液体积是解本题关键,注意容量瓶的选取方法,为易错题.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
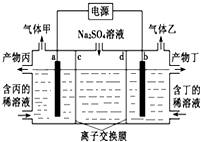 电解硫酸钠溶液生产硫酸和烧碱溶液的装置如下图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是( )
电解硫酸钠溶液生产硫酸和烧碱溶液的装置如下图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是( )| A. | a极与电源的负极相连 | B. | a电极反应式:2H2O+2e-=H2↑+2OH- | ||
| C. | 离子交换膜d为阴离子交换膜 | D. | 产物丙为硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种环保型的新涂料,其合成路线如下图所示:
)是一种环保型的新涂料,其合成路线如下图所示:
 ,E是高分子化台物,其结构简式为
,E是高分子化台物,其结构简式为 ;
; $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O;
+H2O; (写出其中一种的结构简式).
(写出其中一种的结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只要在室内放一盆水 | |
| B. | 向地势低的地方撤离 | |
| C. | 观察风向,顺风撤离 | |
| D. | 用湿毛巾或蘸有弱碱性溶液的毛巾捂住口鼻撤离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com