
下列说法中,正确的是( )
A.NH3是碱性气体,能使酚酞溶液变红色
B.SiO2是酸性氧化物,不溶于任何酸
C.SO2具有漂白性,能使溴水褪色
D.浓H2SO4具有吸水性,能使蔗糖发生炭化
 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:
下列制取硫酸铜的实验设计中,能体现“经济、高效、环保”精神的最佳方案是( )
A.铜与浓硫酸共热
B.用铜片为阳极,石墨为阴极,电解稀硫酸
C.先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解
D.适当温度下,使铜片在持续通入空气的稀硫酸中溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应H2 + Cl2 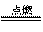 2HCl,下列说法正确的是:( )
2HCl,下列说法正确的是:( )
A.该反应中,化学能只有转变为热能
B.反应物所具有的总能量高于产物所具有的总能量
C.断开1mol H—H键和1mol Cl—Cl键所吸收的总能量小于形成1mol H—Cl键所放出的能量
D.产物所具有的总能量高于反应物所具有的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应:2NO2(g)  2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是( )
2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
A. ①④ B.②③⑤ C.①③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
现有如下两个反应:
A.NaOH + HCl = NaCl + H2O
B.2FeCl3+Cu =2FeCl2+CuCl2
(1)根据两反应本质,能设计成原电池的是:__________(选择“A”或“B”) (1分);
(2)如果可以, 写出负极电极反应式:_______________,电解质溶液:____________;
(3)由第(2)小题可知:一个完整有氧化还原反应方程式可拆写成两个“半反应式”,一个是氧化反应式,一个是还原反应式,并由此实现了化学能与电能的相互转化;则3NO2+H2O = 2H++2NO3-+NO反应的氧化反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种碳架结构如下的烃,下列描述不正确的是( )

A.a和d互为同分异构体
B.b和c是同系物
C.a和d都能发生加成反应
D.b、c、d都能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
1-乙氧基萘常用作香料,也可合成其他香料。实验室制备1-乙氧基萘的过程如下:
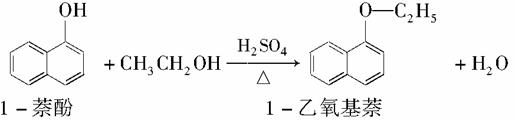
已知:①相关物质的物理常数如下。
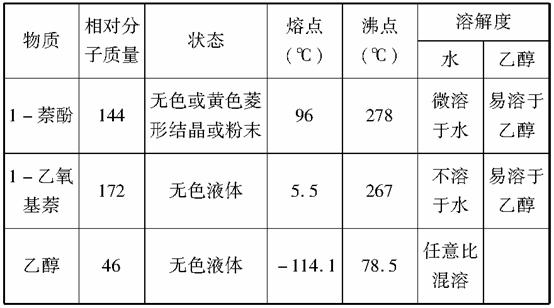
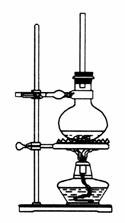
②1-萘酚的性质与苯酚相似,有难闻的苯酚气味,苯酚在空气中易被氧化为粉红色。
请回答以下问题:
(1)将72 g 1-萘酚溶于100 mL无水乙醇中,加入5 mL浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是___________________________________________。
(2)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是________________(填序号)。
A.③②④① B.①②③④ C.②①③④
(3)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图所示,时间延长、温度升高,1-乙氧基萘的产量下降的原因可能是________________。
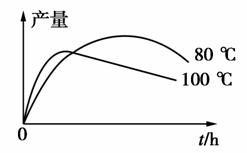
(4)提纯的产品经测定为43 g,本实验中1-乙氧基萘的产率为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某可逆反应X(g)+Y(g)Z(g)+2W(g),其化学平衡常数K和温度的关系如下表:
| T/℃ | 700 | 800 | 850 | 1000 |
| K | 0.01 | 0.05 | 0.10 | 0.40 |
(1)上述反应的平衡常数表达式K=________,ΔH________0(填“>”或“<”)。加入催化剂,该反应的ΔH将________(填“增大”、“减小”或“不变”)。
(2)若上述反应在绝热恒容的密闭容器内进行,则能说明该反应达到化学平衡状态的依据有________。
A.混合气体的密度保持不变
B.v正(X)=v正(Z)
C.容器内温度恒定
D.W的质量分数不变
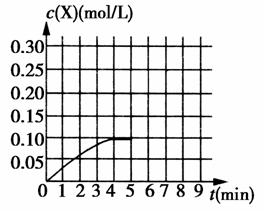
(3)在850 ℃、体积为1 L的密闭容器内,加入0.2 mol Z和0.3 mol W发生上述反应。X的c(X)-t曲线如图所示。
①0~4 min内W的平均速率为________mol·L-1·min-1。
②在5 min末将容器体积缩小至0.5 L,若在8 min末达到新平衡(此时X的浓度约为0.26 mol/L),请在图中画出5 min~9 min的X浓度的变化曲线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com