
分析 滤液中没有Cu2+,说明溶液中也没有Fe3+,则溶液中阳离子有Fe2+和H+,溶质为FeCl2和HCl,
根据电荷守恒得2n(Fe2+)+n(H+)=n(Cl-),则n(Fe2+)=$\frac{4.40mol/L×0.1L-0.40mol/L×0.2L}{2}$mol=0.18mol,生成n(H2)=$\frac{0.896L}{22.4L/mol}$=0.04mol,因为还有盐酸剩余,溶液残留固体是Cu,n(Cu)=$\frac{1.28g/mol}{64g/mol}$=0.02mol,
设Fe的物质的量为xmol、Fe2O3的物质的量为ymol,根据Fe原子守恒得:x+2y=0.18,根据转移电子守恒得2x=0.04×2+0.02×2+2y×1,从而计算n(Fe),根据m=nM计算铁的质量.
解答 解:完全反应后滤液中没有Cu2+,说明溶液中也没有Fe3+,则溶液中阳离子有Fe2+和H+,溶质为FeCl2和HCl,
根据电荷守恒得2n(Fe2+)+n(H+)=n(Cl-),则n(Fe2+)=$\frac{4.40mol/L×0.1L-0.40mol/L×0.2L}{2}$mol=0.18mol,生成n(H2)=$\frac{0.896L}{22.4L/mol}$=0.04mol,因为还有盐酸剩余,溶液残留固体是Cu,n(Cu)=$\frac{1.28g/mol}{64g/mol}$=0.02mol,
设Fe的物质的量为xmol、Fe2O3的物质的量为ymol,
根据Fe原子守恒得:x+2y=0.18
根据转移电子守恒得:2x=0.04×2+0.02×2+2y×1,
解得:x=0.10、y=0.04,
所以原混合物中铁的质量为:m(Fe)=0.10mol×56g/mol=5.6g,
答:原混合物中单质铁的质量为5.6g.
点评 本题考查混合物反应的计算,题目难度中等,试题侧重考查分析计算能力,明确溶液中的溶质是解本题关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的化学计算能力.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅和氯化镁熔化 | B. | 碘和氯化铵受热变成气体 | ||
| C. | 碘和干冰的升华 | D. | 氯化钠和氯化氢溶于水 | ||
| E. | 硅和蔗糖的熔化 | F. | 酒精和水的挥发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②④⑤⑥ | C. | ②③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
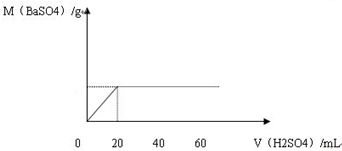
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.4mol/L | D. | 0.8mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
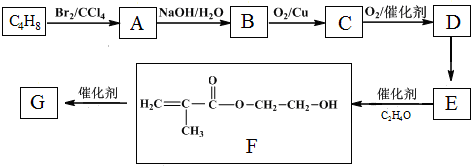
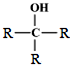 $\stackrel{O_{2}/Cu}{→}$不能被氧化
$\stackrel{O_{2}/Cu}{→}$不能被氧化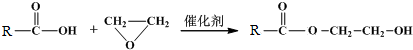
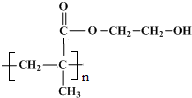 .
.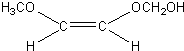 、
、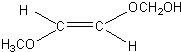 、
、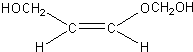 、
、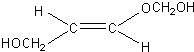 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu $\stackrel{稀HNO_{3}}{→}$Cu(NO3)2 | |
| B. | Cu $\stackrel{Cl_{2}}{→}$CuCl2 $\stackrel{NaOH溶液}{→}$Cu(OH)2 $\stackrel{稀HNO_{3}}{→}$ Cu(NO3)2 | |
| C. | Cu $\stackrel{O_{2}}{→}$CuO$\stackrel{稀HNO_{3}}{→}$ Cu(NO3)2 | |
| D. | Cu $\stackrel{浓H_{2}SO_{4}}{→}$CuSO4 $\stackrel{Ba(NO_{3})_{2}溶液}{→}$ Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
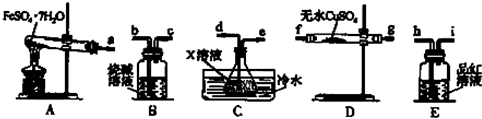
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com