
下列化学反应的离子方程式书写正确的是( )。
A.稀硝酸和过量铁屑反应:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.向硫酸氢铵溶液中加入少量氢氧化钠溶液:NH4++OH-=NH3↑+H2O
C.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D.H2C2O4使酸性KMnO4溶液褪色:5H2C2O4+6H++2MnO4-=10CO2↑+2Mn2++8H2O
科目:高中化学 来源:2014年高考化学题型冲刺练习 突破离子反应的三个角度(解析版) 题型:选择题
在水溶液中能大量共存的一组离子是( )
A.HCO3-、H+、NO3-、Na+
B.Na+、Cu2+、OH-、SO42-
C.Mg2+、H+、AlO2-、SO42-
D.NH4+、K+、Br-、NO3-
查看答案和解析>>
科目:高中化学 来源:2014年高考化学题型冲刺练习 基础实验题(解析版) 题型:选择题
下列对实验现象的解释与结论,正确的是( )
选项 | 实验操作 | 实验现象 | 解释与结论 |
A | 向鸡蛋清溶液中加入 饱和(NH4)2SO4溶液 | 有白色沉淀产生 | 蛋白质变性 |
B | 向某溶液中加入盐酸 酸化的BaCl2溶液 | 有白色沉淀产生 | 该溶液中一定含有SO |
C | 向甲苯中滴入少量浓 溴水,振荡,静置 | 溶液分层,上层呈橙红 色,下层几乎无色 | 甲苯和溴水发生取代反 应,使溴水褪色 |
D | 向蔗糖中加入浓硫酸 | 变黑,放热,体积膨胀, 放出刺激性气体 | 浓硫酸具有脱水性和强 氧化性,反应中生成C、 SO2和CO2等 |
查看答案和解析>>
科目:高中化学 来源:2014年高考化学题型冲刺练习 化学基本概念、解决化学与STSE问题(解析版) 题型:选择题
生活是化学的源泉,下列有关生产、生活中的化学叙述错误的是( )
A.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂
B.变质的植物油有难闻的特殊气味,是由于植物油发生了酯化反应
C.一定浓度的双氧水可用于伤口的消毒
D.采煤工业上,爆破时把干冰和炸药放在一起,既能增强爆炸威力,又能防止火灾
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版专练3限定条件离子共存及离子方程式书写练习卷(解析版) 题型:选择题
下列解释事实的离子方程式不正确的是( )。
A.氨水使酚酞溶液变红:NH4++H2O NH3·H2O+H+
NH3·H2O+H+
B.醋酸使碳酸钙溶【解析】
CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O
C.草酸溶液使酸性高锰酸钾溶液褪色:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
D.向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版专练3限定条件离子共存及离子方程式书写练习卷(解析版) 题型:选择题
常温下,在指定环境中,下列各组离子一定可以大量共存的是( )。
A.使pH试纸呈红色的溶液中:Fe2+、ClO-、SO42-、Na+
B.在pH=3的溶液中:Na+、NO3-、Cl-、Al3+
C.由水电离出的c(H+)=10-13 mol·L-1的溶液中:CO32-、SO42-、Cl-、Na+
D.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版专练3限定条件离子共存及离子方程式书写练习卷(解析版) 题型:选择题
某溶液中存在XO-,且X为短周期元素,则一定能在该溶液中大量共存的离子组是( )。
A.Na+、H+、SO42-、I- B.Na+、Ca2+、CO32-、Al3+
C.Na+、K+、Fe2+、H+ D.K+、SO42-、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习专练2 阿伏加德罗常数的判断练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是( )。
A.3 mol NF3与水完全反应生成HNO3和NO,转移电子数2 NA
B.标准状况下,32 g硫(结构见图)含SS的数目为2 NA
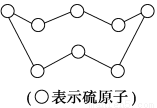
C.标准状况下11.2 L正戊烷所含共用电子对数为8NA
D.含a mol·L-1 H+的醋酸溶液稀释10倍后,H+为0.1aNA
查看答案和解析>>
科目:高中化学 来源:2014年高中化学鲁科版选修四第1章 化学反应与能量转化练习卷(解析版) 题型:填空题
(1)合成氨反应的热化学方程式:N2(g)+3H2(g) 2NH3(g)ΔH=-92.2kJ·mol-1
2NH3(g)ΔH=-92.2kJ·mol-1
已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2 kJ的热量,至少在反应混合物中要投放N2的物质的量为________ mol。
(2)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式:__________________________,
负极的电极反应式:__________________________。
(3)如图是一个电解过程示意图。
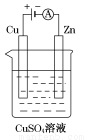
①锌片上发生的电极反应式是:_______________________
②假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为128 g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com