
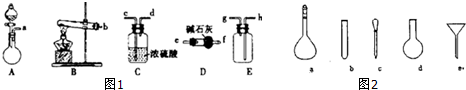
���� ��1��������ȡ�����ӡ��ռ���˳������ʵ��װ�ã�
��2�����ݶ�����̼�Ͱ������ܽ����ж���ͨ������壬�ɷ�Ӧ���������д������ʽ��
��3������Ti��OH��4���ܽ�ƽ�������ܶȻ����������
��4������һ�����ʵ���Ũ�ȵ���Һ������Ҫ����ƿ�ͽ�ͷ�ιܣ�
��5����Ϊ����KSCN��ָʾ�����յ�ʱNH4Fe��SO4��2���ٷ�Ӧ������Ѫ��ɫ��Fe��SCN��3��
��6������n=cV����n��Fe3+�������ݵ���ת���غ����n��Ti3+�����ٸ���Tiԭ���غ����n��TiO2��������m=nM����m��TiO2������������TiO2������������
��7�����ݰ����Ͷ�����̼��ˮ�е��ܽ���жϣ�������ж����ЧӦ��
��� �⣺��1��ʵ������ȡ�������ù��塢���������װ�ã�����ӦѡBΪ��Ӧװ�ã��������к���ˮ���������ڼ������壬����Ӧѡ�������������ˮ��������ѡD��������������ˮ���Ұ������ܶ�С�ڿ������ܶȣ�����Ӧ���������ſ������ռ�����ѡE����װ�ýӿ�˳��Ϊ��befg��h����
��Ҫ��ȡ���ռ��������CO2��Ӧѡ��ACEװ�ã�
�ʴ�Ϊ��befg��h����ACE��
��2��������������ˮ��������̼��������ˮ������Ӧ��ͨ�백������������ˮ���ɰ�ˮ����Һ�ʼ��ԣ�������̼���������壬�ܺͼӦ����̼��泥�̼��狀��Ȼ��Ʒ������ֽⷴӦ����̼��ƺ��Ȼ�泥���Ӧ�ķ���ʽΪ��CaCl2+CO2+2NH3+H2O=CaCO3��+2NH4Cl��
�ʴ�Ϊ��NH3��CaCl2+CO2+2NH3+H2O=CaCO3��+2NH4Cl��
��3�����TiCl4ˮ�����Һ��pH=2��������Һ�е�C��OH-��=10-12mol•L-1��c��Ti4+��=$\frac{Ksp}{{C}^{4}��O{H}^{-}��}$=$\frac{7.94��1{0}^{-54}}{��1{0}^{-12}��^{4}}$mol•L-1=7.94��10-6 mol•L-1��
�ʴ�Ϊ��7.94��10-6mol•L-1��
��4������NH4Fe��SO4��2����Һʱ��ʹ�õ���������ƽ��ҩ�ס����������ձ�����Ͳ�⣬����Ҫ��ͼ2�е�����ƿ�ͽ�ͷ�ιܣ�
�ʴ�Ϊ��ac��
��5��Fe3+��Ti3+��Ӧ������ԭΪFe2+������KSCN���Ժ�ɫ�����ﵽ�ζ��յ�ʱ���ټ���NH4Fe��SO4��2����Һ��Fe3+���������ɺ�ɫ���ζ��յ����������Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ��
�ʴ�Ϊ����Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ��
��6��n��Fe3+��=c mol/L��V��10-3L=cV��10-3mol�����ݵ���ת���غ��֪n��Ti3+��=n��Fe3+��=cV��10-3mol���ٸ���Tiԭ���غ�n��TiO2��=cV��10-3mol����m��TiO2��=cV��10-3mol��Mg/mol=cVM��10-3g����TiO2����������Ϊ$\frac{cVM��1{0}^{-3}g}{wg}$��100%=$\frac{cVM}{10w}$%��
�ʴ�Ϊ��$\frac{cVM}{10w}$%��
��7��������ж����ЧӦ����ȡ������Ʒ��ˮ����γɷ�ɢϵ����һ����Ӳ������䣬�����ֹ�����ͨ·����֤����Ʒ�������������ǣ�
�ʴ�Ϊ��ȡ������Ʒ��ˮ����γɷ�ɢϵ����һ����Ӳ������䣬�����ֹ�����ͨ·����֤����Ʒ�������������ǣ�
���� ������Ҫ�������ʵ��Ʊ�����Һ�����ơ������ⶨ�Ȼ���ʵ���������Ŀ�ѶȲ�����ע��������ʵ�����Ϊ����Ĺؼ���ѧϰ��ע����ۣ���2���ķ�Ӧԭ�������ں����Ƽ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ҫ���ȷ����ķ�Ӧһ�������ȷ�Ӧ | |
| B�� | �κη��ȷ�Ӧ�ڳ�����һ���ܷ��� | |
| C�� | �¶�ѹǿһ��ʱ�����ȵġ������ӷ�Ӧ���Է����� | |
| D�� | ���ȷ�Ӧһ���Ƿ�Ӧ������������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4 | B�� | CuSO4 | C�� | NaCl | D�� | KOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij�¶�ʱpH=6�Ĵ�ˮ�к���10-6NA��H+ | |
| B�� | 7.8g��Na2S��Na2O2�Ļ�����к��е�������������0.1NA | |
| C�� | ��25�桢1.01��105Paʱ��121gCF2Cl2��������ԭ����Ϊ2NA | |
| D�� | �����£�5.6g��Ͷ�뵽������Ũ�����У���Ӧת�Ƶĵ�����Ϊ0.3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ����Ҫ����2mol/Lϡ����250mL��
ʵ����Ҫ����2mol/Lϡ����250mL���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
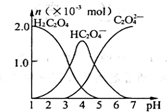 �����£���10mL 0.2mol•L-1���ᣨH2C2O4����Һ����μ����Ũ�ȵ�NaOH��Һ���й��������ʵ���������Һ��pH����ͼ��ϵ������˵����ȷ����
�����£���10mL 0.2mol•L-1���ᣨH2C2O4����Һ����μ����Ũ�ȵ�NaOH��Һ���й��������ʵ���������Һ��pH����ͼ��ϵ������˵����ȷ����| A�� | HC2O4-����Һ��ˮ��̶ȴ��ڵ���̶� | |
| B�� | ��V��NaOH��=10 mL��ʱ����Һ��ˮ�ĵ���̶ȱȴ�ˮ�� | |
| C�� | ��V��NaOH��=15 mL��ʱ����Һ�д��ڣ�c��Na+����c��HC2O4-����c��C2O42-����c��OH-����c��H+�� | |
| D�� | ��V��NaOH��=20 mL��ʱ����Һ�д��ڣ�c��OH-��=c��HC2O4-��+2c��H2C2O4��+c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ��� | ���� | �������� | ��t/�� |
| 1 | 0.1mol•L-1 | 0.05mol•L-1 | 3.5 |
| 2 | 0.1mol•L-1 | 0.1mol•L-1 | x |
| 3 | 0.2mol•L-1 | 0.2mol•L-1 | 14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com